题目内容
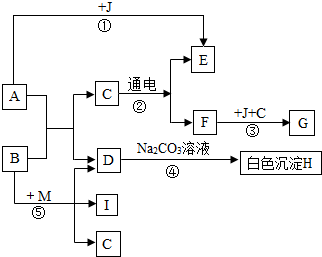
1.已知:A是红色粉末,B、C是氧化物,D、I是常见金属,E为胃酸的主要成分,G为单质.它们之间的转化关系如下:
请回答:
(1)写出物质的化学式:AFe2O3、CCO2.
(2)上述转化①②③中,属于置换反应的有②③(填序号).
(3)为了安全,点燃G气体之前要检验气体的纯度.
(4)写出与上述转化①、③有关反应的化学方程式:①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,③Fe+CuCl2=FeCl2+Cu.
分析 根据E为胃酸的主要成分,所以E是盐酸,A是红色粉末,B、C是氧化物,D是常见金属,D会与盐酸反应生成气体单质,结合一氧化碳和红色的氧化铁在高温的条件下生成铁和二氧化碳,所以A是氧化铁,B是一氧化碳,C是二氧化碳,D是铁,铁和盐酸反应生成氯化亚铁和氢气,所以G是氢气,H是氯化亚铁溶液,铁和氯化铜反应生成铜和氯化亚铁,所以F是氯化铜溶液,I是铜,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)E为胃酸的主要成分,所以E是盐酸,A是红色粉末,B、C是氧化物,D是常见金属,D会与盐酸反应生成气体单质,结合一氧化碳和红色的氧化铁在高温的条件下生成铁和二氧化碳,所以A是氧化铁,B是一氧化碳,C是二氧化碳,D是铁,铁和盐酸反应生成氯化亚铁和氢气,所以G是氢气,H是氯化亚铁溶液,铁和氯化铜反应生成铜和氯化亚铁,所以F是氯化铜溶液,I是铜,经过验证,推导正确,所以A是Fe2O3,C是CO2;
(2)反应①是氧化铁和一氧化碳在高温的条件下反应生成铁和二氧化碳,化学方程式为:Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;②是铁与稀盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl2+H2↑;③是铁和氯化铜溶液反应生成铜和氯化亚铁,化学方程式为:Fe+CuCl2=Cu+FeCl2;置换反应是单质与化合物反应生成另外的一种单质和一种化合物,分析以上三个反应可知,②③是置换反应;
(3)可燃性气体不纯会引起爆炸,因此点燃氢气之前要检验气体的纯度;
(4)反应①是氧化铁和一氧化碳在高温的条件下反应生成铁和二氧化碳,化学方程式为:Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
反应③是铁和氯化铜溶液反应生成铜和氯化亚铁,化学方程式为:Fe+CuCl2=Cu+FeCl2.
故答案为:(1)Fe2O3,CO2;
(2)②③;
(3)检验气体的纯度;
(4)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,Fe+CuCl2=FeCl2+Cu.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 2011年11月,国家环境保护部对外公布《环境空气质量标准》和《环境空气质量指数日报技术规定》征求意见稿,
2011年11月,国家环境保护部对外公布《环境空气质量标准》和《环境空气质量指数日报技术规定》征求意见稿,(1)减少煤、石油和天然气等化石燃料的燃烧,会有助于减少二氧化碳的产生.
化石燃料燃烧时排放出的二氧化硫在空气中反应后的生成物溶于雨水,会形成酸雨.
(2)如图是自然界碳、氧循环简图
a.图中③是自然界中消耗二氧化碳的主要途径,其名称为光合作用.
b.按序号和要求的反应类型完成下列化学方程式
| 序号 | 反应类型 | 化学方程式 |
| ① | 分解反应 | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
| ② | 化合反应 | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
| A. | 钢铁生锈 | B. | 干冰升华 | C. | 食物腐烂 | D. | 铜绿分解 |
| A. | 医用酒精 | B. | 食盐固体 | C. | 醋 | D. | 蔗糖溶液 |
 如图,A、B、C、D、各代表铝、稀盐酸、氧气、硫酸铜溶液四种物质中的一种.常温下,相切物质间能发生反应,不相切物质间不能发生反应且A为单质,D溶液为蓝色
如图,A、B、C、D、各代表铝、稀盐酸、氧气、硫酸铜溶液四种物质中的一种.常温下,相切物质间能发生反应,不相切物质间不能发生反应且A为单质,D溶液为蓝色