题目内容
18.采用适当的试剂,可从石灰石(主要成分是CaCO3)中获得高纯度CaCO3,其流程如下
①流程图中进行的操作2的名称是过滤;
②石灰石煅烧反应的基本反应类型是分解反应.
③该流程图所示物质中,溶于水放出大量热的氧化物是CaO(填“化学式”),该物质与水反应的化学方程式为CaO+H2O═Ca(OH)2.
分析 ①操作2都是将不溶于液体的固体和液体分离;
②石灰石经高温煅烧可制得氧化钙固体和二氧化碳气体,该反应是一种物质分解成为两种物质,符合分解反应类型;
③氧化钙溶于水放出热量,根据方程式的写法写出化学方程式;
解答 解:①操作2都是将不溶于液体的固体和液体分离,可以用过滤的方法;
②石灰石煅烧的反应物是碳酸钙,生成物是氧化钙和二氧化碳,二氧化碳后面标上上升符号,所以化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,该反应是一种物质分解成为两种物质,符合分解反应类型;
③氧化钙溶于水放出热量,反应物是氧化钙和水,生成物是氢氧化钙,所以方程式是:CaO+H2O═Ca(OH)2;
故答案为:
①过滤;②分解反应;③CaO;CaO+H2O═Ca(OH)2
点评 本题难度不是很大,掌握碳酸钙、生石灰与熟石灰之间的转化、理解“绿色化学”的核心理念是正确解答本题的关键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
8.下列是李明在实验室进行氧气的制取、收集、验满和验证性质的操作,其中合理的是( )
| A. | 将高锰酸钾放于试管口向上的试管中进行加热分解 | |
| B. | 将导管口伸到集气瓶的瓶口处,用向下排空气法收集氧气 | |
| C. | 将点燃的木条伸到集气瓶的中间部位进行验满 | |
| D. | 将镁条伸入充满氧气的集气瓶中并点燃,验证氧气的性质 |
9.除去下列各物质中混有的少量杂质,所用试剂或方法错误的是
| 物质 | 杂质 | 试剂或方法 | |
| A | NaOH | Ca(OH)2 | 过量Na2CO3溶液、过滤 |
| B | CH4 | H2O | 通过盛有浓硫酸的洗气瓶 |
| C | FeCl2 | CuCl2 | 过量铁粉、过滤 |
| D | Ca(NO3)2 | CaCl2 | 适量AgNO3、过滤 |
| A. | A | B. | B | C. | C | D. | D |
6. 如图为甲、乙、丙在水中的溶解度曲线图,下列说法正确的是( )
如图为甲、乙、丙在水中的溶解度曲线图,下列说法正确的是( )
 如图为甲、乙、丙在水中的溶解度曲线图,下列说法正确的是( )
如图为甲、乙、丙在水中的溶解度曲线图,下列说法正确的是( )| A. | 三种物质的溶解度都随温度升高而增大 | |
| B. | t1℃时,甲、丙两种物质的溶液中,溶质质量分数相等 | |
| C. | t2℃时,不可能制得相同质量分数的甲、乙、丙溶液 | |
| D. | t3℃时,甲的溶解度为80g |
13.下列几种符号有关说法正确的是( )
①CO2②2O③Ca2+ ⑤Na2SO3⑥ZnSO4.
⑤Na2SO3⑥ZnSO4.
①CO2②2O③Ca2+
 ⑤Na2SO3⑥ZnSO4.
⑤Na2SO3⑥ZnSO4.| A. | ①②中数字“2”表示的意义相同 | |
| B. | ③⑥中金属元素在化合物中的化合价相同 | |
| C. | ③④表示的是阳离子 | |
| D. | ⑤⑥中含有相同的原子团 |
10. 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | t2℃时,a、b、c三种物质的溶解度大小关系是a>b>c | |
| B. | t1℃时,20g a加入到50g水中,充分溶解后得到70g a的饱和溶液 | |
| C. | t1℃时,a、c两物质的饱和溶液中所含的溶质质量一定相等 | |
| D. | t2℃时,将75g的a饱和溶液降温到t1℃,析出15g晶体 |
 哈尔滨是中国第一桶啤酒的生产地.啤酒作为文化载体,在哈尔滨成 为人们社会交往、信息洶通的文化钮带.请回答下列相关问题:
哈尔滨是中国第一桶啤酒的生产地.啤酒作为文化载体,在哈尔滨成 为人们社会交往、信息洶通的文化钮带.请回答下列相关问题: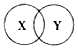 化学概念间有不同的关系,如包含、并列、交叉关系等.下列选项符合如图所示关系的是( )
化学概念间有不同的关系,如包含、并列、交叉关系等.下列选项符合如图所示关系的是( )