题目内容
15.只含铜和氧两种元素的固体样品18g,测得铜的质量为16g.已知铜的氧化物有CuO和Cu2O,请通过分析或计算回答下列问题:(1)固体样品中氧元素的质量为2克;
(2)该样品的组成情况有Cu2O、CuO和Cu(写出所有可能的组成);
(3)若固体样品由两种物质组成,则质量偏少的那种物质的质量分数为$\frac{4}{9}$(用分数表示).
分析 根据题中特点“只含铜和氧两种元素的固体样品”,所以此题主要根据所给固体的质量,及其中铜元素的质量,计算出氧元素的质量;再根据选项中的物质进行计算铜元素的质量分数或质量分数的范围,进行确定.
解答 解:(1)氧元素的质量=18g-16g=2g;
(2)通过计算:固体样品中铜元素的质量分数=$\frac{16g}{18g}$×100%=88.89%;
CuO中铜元素的质量分数=$\frac{64}{64+16}$×100%=80%;
Cu2O中铜元素的质量分数=$\frac{64×2}{64×2+16}$×100%=88.89%.
因为铜的氧化物有CuO和Cu2O,所以该样品的组成情况有CuO和Cu;Cu2O;
(3)若固体样品由两种物质组成,所以该混合物中一定含有铜和Cu2O,其中铜的含量减少.
铜的质量分数80%a+(18g-a)=16g解答x=10g,所以铜为18g-10g=8g,所以铜的质量分数为$\frac{8g}{18g}$=$\frac{4}{9}$.
故答案为:
(1)2;
(2)Cu2O;CuO和Cu;
(3)$\frac{4}{9}$
点评 此题通过元素质量分数的公式计算,又从定量角度进行了范围分析.

练习册系列答案
相关题目
5.小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液,实验过程中加入Na2CO3溶液的质量与产生沉淀或气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液pH的变化关系如图2所示.下列说法中正确的是( )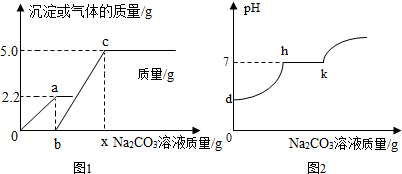

| A. | 图1中0→a段表示生成沉淀的过程 | |
| B. | 图1中a的值为106 | |
| C. | 图1中c点时,溶液中的溶质有两种 | |
| D. | 图1中b→c的反应过程中溶液的pH变化情况可用图2中h→k段曲线表示 |
3.下列有关说法正确的是( )
| A. | 常温下,过氧化氢溶液极易分解产生氧气 | |
| B. | 验满氧气的方法是用带火星的木条靠近集气瓶口 | |
| C. | 配制一定质量分数的NaCl溶液必需的玻璃仪器只有烧杯和玻棒 | |
| D. | 露置在空气中的氢氧化钠,其成分不会发生变化 |
20.为验证甲、乙、丙三种金属的活动性顺序,把三种金属分别放入稀盐酸中,只有乙表面无明显变化,把甲放入丙的硝酸盐溶液中,甲的表面有丙析出,则甲、乙、丙三种金属的活动性顺序由强到弱的是( )
| A. | 丙 甲 乙 | B. | 甲 丙 乙 | C. | 乙 甲 丙 | D. | 丙 乙 甲 |
7.决定元素种类的是( )
| A. | 中子数 | B. | 最外层电子数 | C. | 核外电子数 | D. | 质子数 |
7.下列涉及学科观点的有关说法正确的是( )
| A. | 微粒观:水是由氢原子和氧原子构成的 | |
| B. | 根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化 | |
| C. | 根据结构观:氦原子和镁原子最外层电子数相同,化学性质相似 | |
| D. | 根据守恒观:10mL质量分数40%的硫酸,加l0mL水后质量分数变为20% |

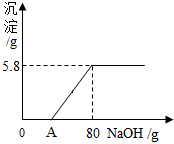 向盛有200g稀盐酸溶液的烧杯中加入一定量的铁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示,请回答:
向盛有200g稀盐酸溶液的烧杯中加入一定量的铁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示,请回答: