题目内容
13. 将 100g 稀盐酸慢慢加入到 24g 含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示.完成以下计算:
将 100g 稀盐酸慢慢加入到 24g 含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示.完成以下计算:(1)石灰石样品中碳酸钙的质量=20g
(2)生成二氧化碳8.8克;
(3)求该稀盐酸的质量分数.
分析 石灰石中的碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳,由图中可知剩余固体质量是4g,说明碳酸钙质量是20g,根据碳酸钙质量可以计算生成二氧化碳的质量和反应的氯化氢质量,进一步可以计算该稀盐酸的质量分数.
解答 解:(1)石灰石样品中碳酸钙的质量为:24g-4g=20g,
固体:20g.
(2)设反应的氯化氢质量为x,生成二氧化碳质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
20g x y
$\frac{100}{20g}$=$\frac{73}{x}$=$\frac{44}{y}$,
x=14.6g,y=8.8g,
故填:8.8.
(3)该稀盐酸的质量分数为:$\frac{14.6g}{80g}$×100%=18.25%,
答:该稀盐酸的质量分数为18.25%.
点评 计算稀盐酸的质量分数时,和碳酸钙恰好完全反应的稀盐酸质量是80g,不是100g,要注意理解.

练习册系列答案
相关题目
3.下列粒子结构示意图中,表示阴离子的是( )
| A. | 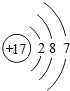 | B. |  | C. |  | D. |  |
4.下列化学式书写不正确的是( )
| A. | 氧化镁 MgO2 | B. | 氧化钠 Na2O | C. | 硫酸锌 ZnSO4 | D. | 氢氧化铜 Cu(OH)2 |
1.将锌片放入下列溶液中,反应后所得溶液的质量比原溶液的质量小的是( )
| A. | 稀H2SO4 | B. | KNO3溶液 | C. | CuSO4溶液 | D. | AgNO3溶液 |
18.下列物质的用途与其化学性质相关的是( )
| A. | 农业上用氯化钠溶液选种 | |
| B. | 生活中用活性炭除去房间中的甲醛 | |
| C. | 农业上用二氧化碳作温室中气体肥料 | |
| D. | 生活中用大理石作装饰材料 |
19.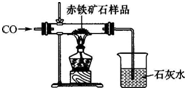 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(2)在利用上图装置进行实验时,小强得到如上两组数据(杂质不参加反应)
你认为他应该选用A(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数;结合装置图回答他不能选用另一组数据计算的原因是石灰水也会吸收空气中的二氧化碳,导致数据m4有误差.
 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)| 反应前 | 氧化铁完全反应后 | |
| A组 | 玻璃管和赤铁矿石样品的质量m1g | 玻璃管和固体物质的质量m2g |
| B组 | 烧杯和澄清石灰水的质量m3g | 烧杯和烧杯中物质的质量m4g |
你认为他应该选用A(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数;结合装置图回答他不能选用另一组数据计算的原因是石灰水也会吸收空气中的二氧化碳,导致数据m4有误差.
 将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.试回答:〔要求(3)、(4)写出计算过程〕
将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.试回答:〔要求(3)、(4)写出计算过程〕