题目内容
1.将锌片放入下列溶液中,反应后所得溶液的质量比原溶液的质量小的是( )| A. | 稀H2SO4 | B. | KNO3溶液 | C. | CuSO4溶液 | D. | AgNO3溶液 |
分析 此题首先分析,把锌加入下列溶液,是否反应.如果不反应,则溶液的质量保持不变;如果反应,再看反应后生成的溶质的质量是否增大或减小,从而判断出溶液的质量的变化.
解答 解:A、根据化学方程式Zn+H2SO4═ZnSO4+H2↑,假设65g锌完全反应,则生成2g氢气,溶液质量增加63g,故错误;
B、锌与硝酸钾溶液不反应,故溶液质量不变,故错误;
C、根据化学方程式Zn+CuSO4═ZnSO4+Cu,假设65g锌完全反应,则生成64g铜,溶液质量增加1g,故错误;
D、根据化学方程式Zn+2AgNO3═Zn(NO3)2+2Ag,假设65g锌完全反应,则生成216g银,溶液质量减少151g,故正确
故选D.
点评 本题考查了物质间发生化学反应时溶液质量的变化,完成此类题目,要明确物质间的反应,以及反应物和生成物的情况,以便能够顺利判断.

练习册系列答案
相关题目
11.下列实验方案能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明某气体是二氧化碳 | 将燃着的木条放入集气瓶中,木条熄灭 |
| B | 证明NaOH溶液部分变质 | 取少量样品,加入过量的氢氧化钙溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞试液 |
| C | 证明燃烧条件之一时温度达到可燃物的着火点 | 将白磷放入80℃热水中,不燃烧,通入氧气后白磷燃烧 |
| D | 证明金属的活动性顺序为Fe>Cu>Ag | 将铜丝浸入AgNO3溶液中,表面析出银白色固体;再将另一根铜丝浸入FeSO4溶液中无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
12.下列关于实验室制取氧气和收集,操作先后顺序中正确的是( )
| A. | 先检查制氧装置的气密性,再装药品 | |
| B. | 先给试管均匀加热,再对着药品加热 | |
| C. | 等导管口排出的气泡连续均匀后,再将导管插入盛水的集气瓶口 | |
| D. | 先熄灭酒精灯,再将导管从水槽中取出 |
9.水是地球上最普遍、最常见的物质之一.下列有关水的说法正确的是( )
| A. | 河水经自来水厂处理后,得到软水 | |
| B. | 水电解实验说明水中含有氢分子和氧分子 | |
| C. | 硬水是混合物,软水是纯净物 | |
| D. | 生活中可用肥皂水检验水的硬度 |
16.质量守恒定律对科学发展具有重大意义
(1)要验证质量守恒定律,下列三个实验不能达到目的是B(填序号).
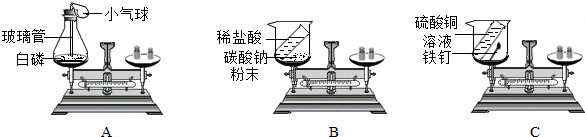
(2)由质量守恒定律可知,化学反应前后一定不变的是①②⑤(填序号).
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质种类
(3)下列物质在密闭容器内反应一段时间,测得反应前后各物质的质量如下
①a 的值为17.
②该反应的基本类型是反应分解反应.
(1)要验证质量守恒定律,下列三个实验不能达到目的是B(填序号).

(2)由质量守恒定律可知,化学反应前后一定不变的是①②⑤(填序号).
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质种类
(3)下列物质在密闭容器内反应一段时间,测得反应前后各物质的质量如下
| 物质 | X | Y | Z | W |
| 反应前质量/g | 12 | 2.2 | 16.2 | 0.9 |
| 反应后质量/g | a | 4.4 | 8.1 | 1.8 |
②该反应的基本类型是反应分解反应.
6.W、X、Y、Z四种物质在一定条件下充分反应后,测得反应前后各物质的质量如表.下列说法错误的是( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 2 | 22 | 34 | 0 |
| 反应后质量/g | 2 | 40 | 待测 | 16 |
| A. | X在反应中可能是催化剂 | B. | 该反应中生成Y的质量为40克 | ||
| C. | 该反应属于分解反应 | D. | 该反应中Z全部参加反应 |
10.确定某种气体的实验室制法,下列因素中:①反应所需的药品及反应条件;②实验装置;③气体收集和放置方法;④气体验满方法;⑤整个反应体系是否环保安全.需要考虑的是( )
| A. | ①③⑤ | B. | ③④⑤ | C. | ①②④⑤ | D. | ①②③④⑤ |
7.有趣的谜语是中华民族灿烂的文化瑰宝.“下完围棋--打一化学名词”,谜底是( )
| A. | 复分解 | B. | 还原 | C. | 分子 | D. | 加成 |
 将 100g 稀盐酸慢慢加入到 24g 含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示.完成以下计算:
将 100g 稀盐酸慢慢加入到 24g 含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示.完成以下计算: