题目内容
8.下列说法正确的是( )| A. | 化合反应一定是氧化反应 | |
| B. | 有氧气参加的反应一定是氧化反应 | |
| C. | 化合反应中,如果有氧气参加,该反应既是化合反应,也是氧化反应 | |
| D. | 氧化反应中一定有氧气参加 |
分析 A、利用两者的概念解决.
B、根据氧化反应定义分析.
C、利用两者的概念解决.
D、化合反应是多变一的反应
解答 解:A、化合反应强调的是反应物与生成物的个数,而氧化反应则是强调的是否与氧的反应,故此选项错误.
B、有氧气参加的反应一定是氧化反应,故此选项正确.
C、化合反应中,如果有氧气参加,该反应既是化合反应,也是氧化反应,故此选项正确.
D、氧化反应不一定有氧气参加,如氢气+氧化铜$\stackrel{加热}{→}$铜+水,该反应中氢气夺取了氧化铜中的氧,发生了氧化反应,故选项说法错误.
故选BC.
点评 此题是对化合反应与氧化反应的考查,解题的关键是抓住两者的概念解题.

练习册系列答案
相关题目
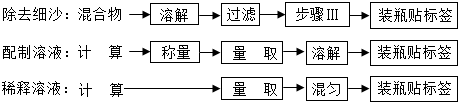
12.炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如图:

(1)操作1把废渣粉碎的目的增大接触面积,使反应充分.
(2)在废渣粉末中加入NaCl多余删掉2的目的是:CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4,写出该反应的化学方程式CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4.
(3)【查阅资料】:不同金属氢氧化物可以多余删掉在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
操作3的名称是过滤,其中用到玻璃棒的作用是引流.在此操作之前,为了使溶液中的Fe3+变成Fe(OH)3沉淀而除去,你认为调节溶液的pH到3.2~4.7(填数值范围)比较合适.
(4)流程图中能循环利用的物质是氯化钠和水.

(1)操作1把废渣粉碎的目的增大接触面积,使反应充分.
(2)在废渣粉末中加入NaCl多余删掉2的目的是:CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4,写出该反应的化学方程式CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4.
(3)【查阅资料】:不同金属氢氧化物可以多余删掉在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
(4)流程图中能循环利用的物质是氯化钠和水.
10.下列有关铁的叙述,错误的是( )
| A. | 生铁是含杂质很多的铁合金 | |
| B. | 铁可以在氧气中燃烧 | |
| C. | 铁跟盐酸反应的化学方程式为:Fe+2HCl=FeCl2+H2↑ | |
| D. | 铁在潮湿的空气中会生锈 |


 如图是初中化学中常见物质间的转化关系,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同.其中“→”表示能生成这种物质,其余反应条件、部分反应物已略去.试推断:
如图是初中化学中常见物质间的转化关系,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同.其中“→”表示能生成这种物质,其余反应条件、部分反应物已略去.试推断: 实验Ⅰ:实验室制O2.
实验Ⅰ:实验室制O2.