题目内容
16.在一个密闭容器内有氧气、二氧化碳、水蒸汽和未知纯净物W,在一定条件下充分反应,测得反应前后各物质的质量如表:| 物质 | 氧气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量(g) | 50 | 1 | 1 | 23 |
| 反应后质量(g) | 2 | 45 | 28 | x |
分析 根据质量守恒定律和表格中的数据可得出反应后X的值,分析各物质在反应前后的变化量,若反应后质量减少,则为该反应的反应物;若反应后质量增加,则为反应的生成物.
解答 解:根据质量守恒定律,x=(50+1+1+23)g-(2+45+28)g=0;反应后氧气、w的质量减小,属于反应物,二氧化碳、水蒸气的质量增加,属于生成物.
故填:0;二氧化碳、水蒸气.
点评 该题要求学生要掌握好质量守恒定律并能灵活的加以运用,然后会从图表数据中挖掘出有用的数据进行处理计算.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
6.下列除杂设计(括号内为杂质)所选试剂和操作都正确的是( )
| 序号 | 物质 | 选用试剂 | 操作 |
| A | FeCl2溶液(CuCl2溶液) | 过量的铁粉 | 蒸发结晶 |
| B | KClO3固体(KCl) | 加热至不再产生气体 | |
| C | KNO3溶液(KOH) | CuSO4溶液 | 加入适量试剂,过滤、蒸发 |
| D | MgCl2溶液(NaCl) | ①KOH溶液 ②稀盐酸 | 加入过量试剂①,过滤、洗涤 向所得固体中加入适量试剂②至固体恰好溶解 |
| A. | A | B. | B | C. | C | D. | D |
4.某物质的空气中完全燃烧后的产物是二氧化碳和水,则下列关于该物质的元素组成正确的是( )
| A. | 只含碳元素、氢元素 | B. | 只含氢元素 | ||
| C. | 含碳、氢元素,还可能含氧元素 | D. | 一定含氧元素 |
8.下列有关实验室制取氧气的叙述中不正确的是( )
| A. | 在过氧化氢溶液的分解反应中,二氧化锰起催化作用 | |
| B. | 如不使用催化剂,仅加热氯酸钾不会产生氧气 | |
| C. | 用带火星的木条放在瓶口,即可检验一集气瓶中是否充满氧气 | |
| D. | 实验室用氯酸钾和少量高锰酸钾混合加热,也可较快的制取氧气 |
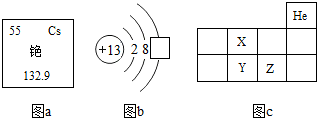 图a 是铯元素在元素周期表中的信息,图b 是铝原子结构示意图,图C 为元素周期表的一部分,X、Y、Z 代表三种不同元素.
图a 是铯元素在元素周期表中的信息,图b 是铝原子结构示意图,图C 为元素周期表的一部分,X、Y、Z 代表三种不同元素.