题目内容
金属与氧气的反应
(1)镁、铝在常温下就能反应,其化学方程式分别为 ; .
(2)铁、铜在温度较高时能与氧气反应,其化学方程式分别为: ; .
(3)“真金不怕火炼”是金在高温下也不与 反应,说明了金的化学性质 .
(4)铝抗腐蚀性好的原因是 .
(1)镁、铝在常温下就能反应,其化学方程式分别为
(2)铁、铜在温度较高时能与氧气反应,其化学方程式分别为:
(3)“真金不怕火炼”是金在高温下也不与
(4)铝抗腐蚀性好的原因是
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:金属可以与氧气发生反应,反应生成金属氧化物;不同的金属与氧气反应时反应的条件不同,如比较活泼的金属镁、铝、锌等在常温下就可以与空气中的氧气反应,生成的氧化物形成一层致密的膜覆盖在金属表现,防止多心进一步与氧气反应;而一些活动性较弱的金属则需要加温才能与氧气反应,如铜、汞等,还有的金属即使在高温下也不与氧气反应,如黄金,真金不怕火炼就是这个道理.
解答:(1)比较活泼的金属镁、铝等在常温下就可以与空气中的氧气反应,故化学方程式分别为:2Mg+O2═2MgO; 4Al+3O2═2Al2O3.
(2)铁在氧气中可以燃烧,火星四溅、放出大量热、生成一种黑色固体四氧化三铁;
铜在加热能与氧气反应生成氧化铜,观察到红色黑变成了黑色粉末氧化铜;故化学方程式分别为
故答:3Fe+2O2
Fe3O4,2Cu+O2
2CuO;
(3)金是活动性最弱的金属,即使在高温下也不与氧气反应,说明化学性质稳定.
(4)铝抗腐蚀性好的原因是:铝在空气中能被氧气氧化生成一层致密的氧化铝保护膜,防止铝进一步被氧化.
故答案为:(1)2Mg+O2═2MgO; 4Al+3O2═2Al2O3.
(2)3Fe+2O2
Fe3O4; 2Cu+O2
2CuO.
(3)氧气,不活泼.
(4)铝在空气中能被氧气氧化生成一层致密的氧化铝保护膜,防止铝进一步被氧化.
(2)铁在氧气中可以燃烧,火星四溅、放出大量热、生成一种黑色固体四氧化三铁;
铜在加热能与氧气反应生成氧化铜,观察到红色黑变成了黑色粉末氧化铜;故化学方程式分别为
故答:3Fe+2O2
| ||
| ||
(3)金是活动性最弱的金属,即使在高温下也不与氧气反应,说明化学性质稳定.
(4)铝抗腐蚀性好的原因是:铝在空气中能被氧气氧化生成一层致密的氧化铝保护膜,防止铝进一步被氧化.
故答案为:(1)2Mg+O2═2MgO; 4Al+3O2═2Al2O3.
(2)3Fe+2O2
| ||
| ||
(3)氧气,不活泼.
(4)铝在空气中能被氧气氧化生成一层致密的氧化铝保护膜,防止铝进一步被氧化.
点评:本题考查了金属与氧气反应的难易程度与金属的活动顺有关,活动性强的金属与氧气反应速度快.

练习册系列答案
相关题目
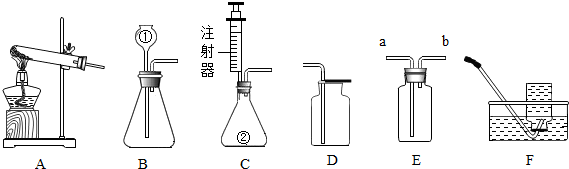
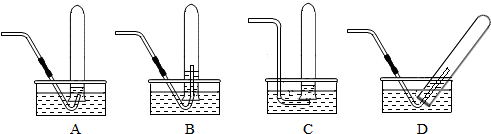
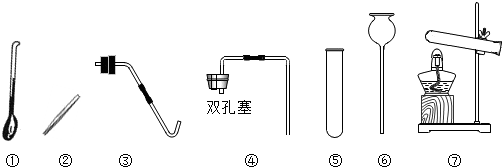
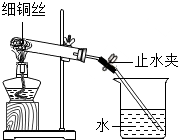 某兴趣小组的同学用如图装置测定空气中氧气的含量.实验过程是:
某兴趣小组的同学用如图装置测定空气中氧气的含量.实验过程是: 如图所示,在室温下的不饱和硝酸钾溶液中放置一个塑料小球.
如图所示,在室温下的不饱和硝酸钾溶液中放置一个塑料小球.