题目内容
在一定温度下,将某Na2SO4溶液恒温蒸发10克水,得到晶体沉淀3克,若将该溶液恒温蒸发20克水,则析出晶体7克,则下列说法正确的是( )
| A、原溶液一定是饱和溶液 |
| B、该温度下,Na2SO4溶液的溶解度是20克 |
| C、原溶液的质量分数为23% |
| D、若将原溶液恒温蒸发15克水,会析出5克晶体 |
考点:晶体和结晶的概念与现象,固体溶解度的概念,溶质的质量分数
专题:溶液、浊液与溶解度
分析:根据题目信息可知,析出晶体以后溶液就饱和了,比较两次蒸发可以发现,说明20克水和5克晶体组成的溶液是饱和溶液,然后根据溶解度的概念写出关系式即可.
解答:解:根据题目信息可知,析出晶体以后溶液就饱和了,比较两次蒸发可以发现,说明20克水和7克晶体组成的溶液是饱和溶液,设物质的溶解度是S.
=
得:S=35克;故B错误;
∵从第二次蒸发水可以看出,每蒸发10克水,就会析出晶体3.5克;每蒸发5克水,就会析出晶体1.75克;但是第一次蒸发掉10克水,就析出晶体3克,说明原来溶液不是饱和溶液,故A错误.
若将原溶液恒温蒸发15克水,会析出3g+1.75g=4.75g克晶体;故D错误.
故选C.
| S |
| 100 |
| 7g |
| 20g |
∵从第二次蒸发水可以看出,每蒸发10克水,就会析出晶体3.5克;每蒸发5克水,就会析出晶体1.75克;但是第一次蒸发掉10克水,就析出晶体3克,说明原来溶液不是饱和溶液,故A错误.
若将原溶液恒温蒸发15克水,会析出3g+1.75g=4.75g克晶体;故D错误.
故选C.
点评:这个题的关键是找出饱和溶液的关系式,即20克水和7克晶体组成的溶液是饱和溶液.

练习册系列答案
相关题目
苹果中富含苹果酸,苹果酸的化学式为C4H4O4.下列说法正确的是( )
| A、苹果酸分子中含有12个原子 |
| B、苹果酸的相对分子质量为116g |
| C、苹果酸中碳元素的质量分数与氢元素的质量分数比为1:1 |
| D、苹果酸中C、H、O三元素的质量比为4:4:4 |
铁是生产和生活中使用最多的金属材料,下列关于铁的叙述错误的是( )
| A、铁生锈时生成四氧化三铁 |
| B、表面涂漆以防止铁生锈 |
| C、铁制品应放置于干燥的环境中 |
| D、保持铁器表面洁净有利于防止铁生锈 |
如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
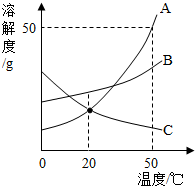

| A、50℃时,三种物质的溶解度由大到小的顺序是A>B>C |
| B、50℃时,把50gA放入50g水中能形成75gA的饱和溶液 |
| C、将C的饱和溶液变为不饱和溶液,可采用降温的方法 |
| D、分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液仍然都是饱和溶液 |
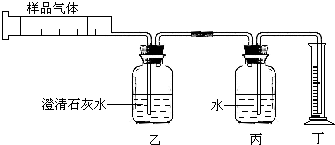 某课外活动小组,欲测定一待旅游开发的溶洞空气中二氧化碳的体积分数,进行如下实验:
某课外活动小组,欲测定一待旅游开发的溶洞空气中二氧化碳的体积分数,进行如下实验: