题目内容
7.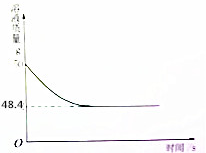 双氧水是过氧化氢的水溶液,它由杀菌消毒的作用,国家标准H2O2的质量百分含量不低于3%,小军从家中拿来一瓶医用过氧化氢溶液.和同学们一起测定溶质质量分数,他们取出该溶液50g,加入适量二氧化锰2g,反应后溶液的质量与反应时间的关系如图所示.
双氧水是过氧化氢的水溶液,它由杀菌消毒的作用,国家标准H2O2的质量百分含量不低于3%,小军从家中拿来一瓶医用过氧化氢溶液.和同学们一起测定溶质质量分数,他们取出该溶液50g,加入适量二氧化锰2g,反应后溶液的质量与反应时间的关系如图所示.(1)H2O2中氢元素的质量分数为94.1%;
(2)完全反应后生成氧气的质量为1.6g;
(3)通过计算得出该双氧水是够达标.
分析 过氧化氢在二氧化锰的催化作用下生成水和氧气,根据质量守恒定律,溶液的减少的质量即生成的氧气质量,据此根据反应的化学方程式列式计算出参加反应过氧化氢的质量,进而计算出该双氧水是够达标.
解答 解:(1)H2O2中氢元素的质量分数为$\frac{16×2}{1×2+16×2}×$100%≈94.1%.
(2)完全反应后生成氧气的质量为50g-48.4g=1.6g.
(3)设参加反应过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{32}=\frac{x}{1.6g}$ x=3.4g
该双氧水中溶质的质量分数为$\frac{3.4g}{50g}$×100%=1.7%.
1.7%小于3%,故不达标.
答:(1)94.1%;(2)1.6g;(3)该双氧水不达标.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
15.刘虹琳同学的化学归纳本上有如下记录,你认为不正确的是( )
| A. | 雨在形成和降落过程中,因吸收并溶解了空气中的二氧化硫而使酸性增强 | |
| B. | 粗盐提纯的一般步骤:溶解--过滤--蒸发--计算产率 | |
| C. | 煤是三大化石燃料之一,其主要成分碳在燃烧的过程中发生了氧化反应 | |
| D. | 氦原子的最外层电子数是2,易失去电子,属于金属元素 |
12.关于石墨烯的认识错误的是( )
| A. | 构成:碳原子 | B. | 结构:微粒排列方式不同于金刚石 | ||
| C. | 性质:可燃性 | D. | 用途:用作超轻绝缘材料 |
16.在厨房里发生的下列变化,不属于化学变化的是( )
| A. | 铁锅生锈 | B. | 天然气燃烧 | C. | 水分蒸发 | D. | 米饭变质 |
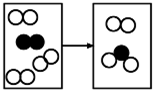 如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子.
如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子. B.
B. C.
C.
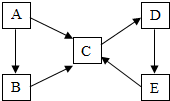 已知A、B、C、D、E五种物质均为初中化学常见物质,都含有同一种元素,它们之间的转化关系如图所示.
已知A、B、C、D、E五种物质均为初中化学常见物质,都含有同一种元素,它们之间的转化关系如图所示.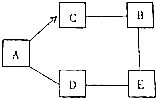 A~E为初中化学常见的五种物质,其类别各不相同,它们相互间的关系如图所示(“→”表示转化关系,“-”表示相互之间会反应).已知A是胃酸中含有的一种酸,C是氧化物,E的溶液呈蓝色.A、B、C、D、E的相对分分数依次增大.(部分反应物、生成物及反应条件已略去)
A~E为初中化学常见的五种物质,其类别各不相同,它们相互间的关系如图所示(“→”表示转化关系,“-”表示相互之间会反应).已知A是胃酸中含有的一种酸,C是氧化物,E的溶液呈蓝色.A、B、C、D、E的相对分分数依次增大.(部分反应物、生成物及反应条件已略去)