题目内容
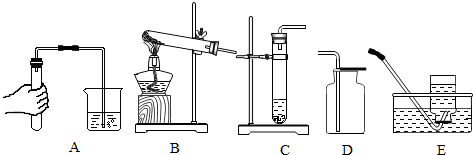
甲同学将燃烧的钠迅速伸入到盛有纯净干燥的CO2的集气瓶中,发现金属钠在CO2中继续燃烧,燃烧停止后,在集气瓶底发现有黑色颗粒生成,瓶内壁上有白色物质生成.
(1)甲认为黑色颗粒是 (用化学式填空),白色物质可能是Na2O或Na2CO3;乙同学认为白色物质还有可能是氢氧化钠固体.甲同学认为乙同学的猜想不正确,其理由是 ;
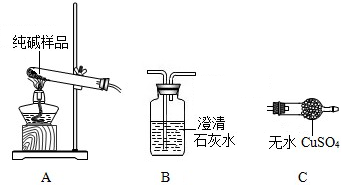
(2)查阅资料发现:氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O=2NaOH.甲同学据此对白色物质进行了如表实验:
(3)丙同学认为方案1得到的结论不正确,理由是:
(4)钠在二氧化碳中燃烧的化学方式为: ,属于基本反应类型中的 反应.
(1)甲认为黑色颗粒是
(2)查阅资料发现:氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O=2NaOH.甲同学据此对白色物质进行了如表实验:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量白色物质于试管中,加入适量水振荡,样品全部溶于水,向其加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(4)钠在二氧化碳中燃烧的化学方式为:
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,反应类型的判定,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据碳是黑色的固体颗粒以及质量守恒定律进行解答;
(2)根据碳酸钠和氯化钙溶液反应生成碳酸钙白色沉淀和氯化钠,氯化钠和氯化钙溶液呈中性进行解答;
(3)根据碳酸钠溶液也呈碱性,也能使无色酚酞试液变红进行解答;
(4)根据实验探究可知钠在二氧化碳中燃烧生成碳酸钠和碳进行解答.
(2)根据碳酸钠和氯化钙溶液反应生成碳酸钙白色沉淀和氯化钠,氯化钠和氯化钙溶液呈中性进行解答;
(3)根据碳酸钠溶液也呈碱性,也能使无色酚酞试液变红进行解答;
(4)根据实验探究可知钠在二氧化碳中燃烧生成碳酸钠和碳进行解答.
解答:解:(1)碳是黑色的固体颗粒,所以黑色颗粒是碳;由质量守恒定律可知,反应物中没有氢元素,所以白色物质不可能是氢氧化钠固体;故填:C;反应物中没有氢元素;
(2)碳酸钠和氯化钙溶液反应生成碳酸钙白色沉淀和氯化钠,氯化钠和氯化钙溶液呈中性,所以取样品少量白色物质于试管中,加入适量水振荡,样品全部溶于水,向其加入过量的CaCl2溶液,出现白色沉淀;静置片刻,取上层清液于试管中,滴加无色酚酞试液,无明显现象,说明白色物质是碳酸钠;故填:Na2CO3;
(3)碳酸钠溶液也呈碱性,也能使无色酚酞试液变红,所以取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液,溶液变成红色,不能确定是氧化钠;故填:碳酸钠溶液也呈碱性;
(4)实验探究可知钠在二氧化碳中燃烧生成碳酸钠和碳,的化学方式为:4Na+3CO2
2Na2CO3+C,该反应是单质和化合物反应生成另外的单质和化合物,属于置换反应.故填:4Na+3CO2
2Na2CO3+C;置换.
(2)碳酸钠和氯化钙溶液反应生成碳酸钙白色沉淀和氯化钠,氯化钠和氯化钙溶液呈中性,所以取样品少量白色物质于试管中,加入适量水振荡,样品全部溶于水,向其加入过量的CaCl2溶液,出现白色沉淀;静置片刻,取上层清液于试管中,滴加无色酚酞试液,无明显现象,说明白色物质是碳酸钠;故填:Na2CO3;
(3)碳酸钠溶液也呈碱性,也能使无色酚酞试液变红,所以取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液,溶液变成红色,不能确定是氧化钠;故填:碳酸钠溶液也呈碱性;
(4)实验探究可知钠在二氧化碳中燃烧生成碳酸钠和碳,的化学方式为:4Na+3CO2
| ||
| ||
点评:此题有一定的综合性,考查了判断物质种类的方法及检验物质的方法.这就要求学生记住一些常见性质,同时也要学会设计一些简单实验判定物质种类.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
下列说法正确的是( )
| A、测某酸性溶液的pH时,先用水将pH试纸润湿 |
| B、电解水时正极产生的气体体积比负极产生的气体体积大 |
| C、相同原子可能构成不同的分子 |
| D、只含有一种元素的物质一定是纯净物 |
 如图甲、乙两个装置均可通过胶头滴管向锥形瓶中滴加某种液体,达到使气球鼓起起的目的,锥形瓶和胶头滴管放入物质正确的一组是( )
如图甲、乙两个装置均可通过胶头滴管向锥形瓶中滴加某种液体,达到使气球鼓起起的目的,锥形瓶和胶头滴管放入物质正确的一组是( )