题目内容
7. 请用所学的化学知识解释下列现象.
请用所学的化学知识解释下列现象.(1)如图用铜丝圈罩在燃着的蜡烛上,蜡烛很快熄灭,其原因是铜丝会吸收热量,导致温度降到蜡烛的着火点以下,从而蜡烛熄灭;
(2)把生石灰放入塑料瓶中,加水井盖上瓶盖振荡,这么做很危险,易出现炸裂而伤人,其原因是生石灰与水反应生成的氢氧化钙具有腐蚀性,且反应过程中放出大量的热,使瓶内气体体积膨胀,导致塑料瓶炸裂;
(3)8•12天津港的第二次爆炸可能是由存放的硝酸铵引发的,因为硝酸铵在400℃时会发生分解,产生氮气、二氧化氮和水,并放出大量热,写出该反应的化学方程式:4NH4NO3$\frac{\underline{\;400℃\;}}{\;}$3N2↑+2NO2↑+8H2O.
分析 (1)根据已有的燃烧的条件进行分析解答,燃烧需要可燃物与氧气接触且温度达到可燃物的着火点,据此解答.
解答 解:(1)将一根铜丝烧成螺旋状网罩罩在一支燃着蜡烛的火焰处,铜丝会吸收热量,导致温度降到蜡烛的着火点以下,从而蜡烛熄灭.
(2)生石灰与水反应生成的氢氧化钙具有腐蚀性,且反应过程中放出大量的热,使瓶内气体体积膨胀,导致塑料瓶炸裂;
(3)硝酸铵在400℃时会发生分解,产生氮气、二氧化氮和水,该反应的化学方程式:4NH4NO3$\frac{\underline{\;400℃\;}}{\;}$3N2↑+2NO2↑+8H2O;
故填:(1)铜丝会吸收热量,导致温度降到蜡烛的着火点以下,从而蜡烛熄灭;(2)生石灰与水反应生成的氢氧化钙具有腐蚀性,且反应过程中放出大量的热,使瓶内气体体积膨胀,导致塑料瓶炸裂;(3)4NH4NO3$\frac{\underline{\;400℃\;}}{\;}$3N2↑+2NO2↑+8H2O.
点评 本题考查的是燃烧与灭火的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
18.如图1是燃气热水器示意图.

(1)某热水器以天然气为燃气.
①写出天然气完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
②当“空气进气孔”被部分堵塞,燃烧将产生有毒气体M,M的化学式为CO.
(2)1kg不同燃料燃烧产生CO2和SO2的质量如表所示.
①其中使用煤作燃料时最易形成酸雨.
②酸雨形成过程中某一步反应的微观示意图如图2,则参加反应中“ ”和“
”和“ ”的分子个数比为1:5.
”的分子个数比为1:5.

| 燃料 | 燃烧产物质量/g | |
| CO2 | SO2 | |
| 汽油 | 2900 | 5.0 |
| 天然气 | 2500 | 0.1 |
| 煤 | 2500 | 11.0 |
①写出天然气完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
②当“空气进气孔”被部分堵塞,燃烧将产生有毒气体M,M的化学式为CO.
(2)1kg不同燃料燃烧产生CO2和SO2的质量如表所示.
①其中使用煤作燃料时最易形成酸雨.
②酸雨形成过程中某一步反应的微观示意图如图2,则参加反应中“
 ”和“
”和“ ”的分子个数比为1:5.
”的分子个数比为1:5.
15.八月桂花开,香气四溢,产生这种现象的原因是( )
| A. | 分子不断运动 | B. | 分子间有间隙 | C. | 分子分成原子 | D. | 分子体积很小 |
12.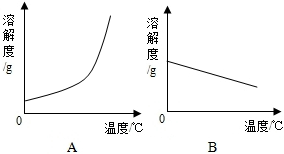 如表是Ca(OH)2和NaOH的溶解度数据,请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据,请回答下列问题:
(1)依据如表数据,绘制Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是A(填A或B).
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.
其中措施正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(3)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为9.1g.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数 乙<甲(填“>”、“<”或“=”).
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.
 如表是Ca(OH)2和NaOH的溶解度数据,请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据,请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.
其中措施正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(3)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为9.1g.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数 乙<甲(填“>”、“<”或“=”).
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.
19.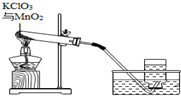 某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g (O:16 Cl:35.5 K:39)
某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g (O:16 Cl:35.5 K:39)
(1)表格中数值a为18.4g.
(2)共制得氧气9.6g.
(3)计算所得氯化钾溶液的溶质质量分数.
 某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g (O:16 Cl:35.5 K:39)
某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g (O:16 Cl:35.5 K:39)| 加热时间/min | 0 | t1 | t2 | t3 | t4 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | a | 18.4 |
(2)共制得氧气9.6g.
(3)计算所得氯化钾溶液的溶质质量分数.
16.化学与生活密切相关,下列说法正确的是( )
| A. | 利用溶解原理,洗洁精能洗去餐具表面的油污 | |
| B. | 察觉燃气泄漏要关闭阀门,开窗通风 | |
| C. | 铵态氮肥与熟石灰混合使用可以明显提高肥效 | |
| D. | 维生素B缺乏会引起夜盲症. |
17.下列各组物质按酸、碱、单质、氧化物顺序排列的是( )
| A. | H2SO4 Na2O C CO | B. | Mg(OH)2 CuSO4 C CO2 | ||
| C. | KOH HNO3 O2 SO3 | D. | HCl NaOH O2 P2O5 |
 (1)有H、C、O、Na四种元素,请选用其中一种或几种元素填写符合下列要求的化学式(各写一个):
(1)有H、C、O、Na四种元素,请选用其中一种或几种元素填写符合下列要求的化学式(各写一个):