题目内容
19.小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%.小明想,这瓶白醋中醋酸的含量是否与标签的标注相符呢?小明用有关酸碱的知识,定量测定白醋中醋酸的含量.【实验原理】
(1)用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:CH3COOH+NaOH=CH3COONa+H2O.
(2)在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05mL,对测定结果的影响很小,可忽略不计.
【实验步骤】
(1)用量筒(填一种仪器名称)量取15.0mL白醋(密度近似为1.0g/mL),倒入烧杯中,再加入20mL蒸馏水稀释.然后滴加2滴无色酚酞试液.
(2)量取45.0mL溶质质量分数为1.0%的氢氧化钠溶液(密度近似为1.0g/mL),用胶头滴管取该氢氧化钠溶液,逐滴地滴加到稀释后的白醋中,同时不断地搅拌烧杯中的溶液,直到恰好完全反应,剩余氢氧化钠溶液5.0mL.
【交流反思】
(3)小明在实验步骤中加适量水稀释白醋,对实验结果有无影响?为什么?
答:无影响,这是因为醋酸质量不变.
(4)小明根据溶液变红色(填写实验现象)确定醋酸和氢氧化钠已完全中和?
【数据处理】根据实验数据,通过计算判断白醋中醋酸的含量是否与标签的标注相符?
分析 醋酸和氢氧化钠反应生成醋酸钠和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:【实验步骤】
(1)用量筒量取15.0mL白醋(密度近似为1.0g/mL),倒入烧杯中,再加入20mL蒸馏水稀释.然后滴加2滴无色酚酞试液.
故填:量筒.
【交流反思】
(3)小明在实验步骤中加适量水稀释白醋,对实验结果无影响,这是因为稀释前后醋酸质量不变.
故填:无影响,这是因为醋酸质量不变.
(4)溶液变红色时,可以确定醋酸和氢氧化钠已完全中和.
故填:溶液变红色.
【数据处理】
设醋酸质量为x,
反应的氢氧化钠质量为:( 45.0mL-5.0mL)×1.0g/mL×1.0%=0.4g,
CH3COOH+NaOH=CH3COONa+H2O,
60 40
x 0.4g
$\frac{60}{x}$=$\frac{40}{0.4g}$,
x=0.6g,
白醋中醋酸的含量为:$\frac{0.6g}{15.0mL×1.0g/mL}$×100%=4%,
由计算可知,白醋中醋酸的含量与标签的标注不相符,
答:白醋中醋酸的含量与标签的标注不相符.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.在生活中处处有化学,在实际生活中下列物质的用途与其化学性质无关的是( )
| A. | 用稀盐酸除热水瓶中的水垢 | B. | 用干冰进行人工降雨 | ||
| C. | 用熟石灰改良酸性土壤 | D. | 用木炭烤肉串 |
14.小明在学校科技节上表演了“化学魔术”,他先用蘸有无色酚酞的笔在白纸上写字,把纸晾干.表演时选用一种无色溶液喷洒在纸上,立即显示出红色的字.他可以选用以下( )溶液.
| A. | 氯化钠溶液 | B. | 氢氧化钠溶液 | C. | 硫酸溶液 | D. | 盐酸 |
4.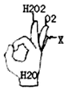 如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )
如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )
 如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )
如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )| A. | CuO | B. | CO | C. | CH4 | D. | H2CO3 |
11.物质的性质决定其用途,下列因果关系不成立的是( )
| A. | 稀有气体化学性质稳定,可用作保护气 | |
| B. | 熟石灰呈碱性,可用来改良酸性土壤 | |
| C. | 干冰升华吸热,可用于人工降雨 | |
| D. | 洗洁精具有乳化作用,可用来除水壶中的水垢 |
8.下列判断正确的是( )
| A. | 合金至少由两种金属熔合而成 | |
| B. | 不同种元素最本质的区别是质子数不同 | |
| C. | 饱和溶液变成不饱和溶液,其溶质质量分数一定变小 | |
| D. | 两种化合物相互作用生成另外两种化合物的反应一定是复分解反应 |