题目内容
某校化学兴趣小组用含杂质的氯化镁(杂质不溶于水,也不参加反应),进行如图所示的实验.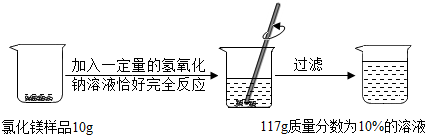
请根据以上信息计算(计算结果精确到0.1%)
(1)实验最终所得的纯净溶液中溶质的质量 g;
(2)恰好完全反应生成沉淀的质量 g;
(3)样品中氯化镁的质量分数和所加入氢氧化钠溶液的质量分数(写出计算过程).

请根据以上信息计算(计算结果精确到0.1%)
(1)实验最终所得的纯净溶液中溶质的质量
(2)恰好完全反应生成沉淀的质量
(3)样品中氯化镁的质量分数和所加入氢氧化钠溶液的质量分数(写出计算过程).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:最终所得的纯净溶液是氯化钠溶液,根据氯化钠的质量利用化学方程式可以求出氢氧化镁的质量、样品中氯化镁的质量以及氢氧化钠溶液中氢氧化钠的质量,进而求氯化镁的质量分数以及氢氧化钠的质量分数.
解答:解:(1)最终所得的纯净溶液是氯化钠溶液,溶质的质量=117g×10%=11.7g;
故答案为:11.7;
设样品中氯化镁的质量为x,消耗氢氧化钠的质量为y,生成氢氧化镁的质量为z
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 80 58 117
x y z 11.7g
=
=
=
x=9.5g,y=8g,z=5.8g
(2)恰好完全反应生成沉淀的质量为5.8g;
故答案为:5.8;
(3)样品中氯化镁的质量分数是:
×100%=95%;
答:样品中氯化镁的质量分数是95%;
(4)氢氧化钠溶液的质量=117g+5.8g-9.5g=113.3g
则加入的氢氧化钠溶液中溶质的质量分数为:
×100%=7.1%
答:氢氧化钠溶液中溶质的质量分数为7.1%.
故答案为:11.7;
设样品中氯化镁的质量为x,消耗氢氧化钠的质量为y,生成氢氧化镁的质量为z
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 80 58 117
x y z 11.7g
| 95 |
| x |
| 80 |
| y |
| 58 |
| z |
| 117 |
| 11.7g |
x=9.5g,y=8g,z=5.8g
(2)恰好完全反应生成沉淀的质量为5.8g;
故答案为:5.8;
(3)样品中氯化镁的质量分数是:
| 9.5g |
| 10g |
答:样品中氯化镁的质量分数是95%;
(4)氢氧化钠溶液的质量=117g+5.8g-9.5g=113.3g
则加入的氢氧化钠溶液中溶质的质量分数为:
| 8g |
| 113.3g |
答:氢氧化钠溶液中溶质的质量分数为7.1%.
点评:本题的难点是如何根据质量守恒定律计算氢氧化钠溶液的质量.

练习册系列答案
相关题目
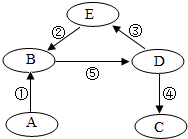 已知A、B、C、D、E五种物质都有人体内含量最高的一种金属元素,其中A是单质,B、C含有两种元素,D、E含有三种元素,反应⑤是放热反应,它们之间的转化关系如图所示,下列推理不正确的是( )
已知A、B、C、D、E五种物质都有人体内含量最高的一种金属元素,其中A是单质,B、C含有两种元素,D、E含有三种元素,反应⑤是放热反应,它们之间的转化关系如图所示,下列推理不正确的是( )| A、E是碳酸钙 |
| B、反应④一定是中和反应 |
| C、反应③可以由多个化学反应实现 |
| D、反应②是吸热反应 |

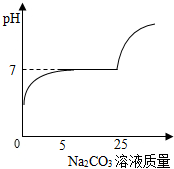 某同学将为了测定实验室制取二氧化碳后的废液中的成分及含量,他将废液过滤,然后取滤液10.0g,向其中滴加10.6%的碳酸钠溶液,并测定溶液的pH,绘制图象如图:
某同学将为了测定实验室制取二氧化碳后的废液中的成分及含量,他将废液过滤,然后取滤液10.0g,向其中滴加10.6%的碳酸钠溶液,并测定溶液的pH,绘制图象如图: A~H是初中化学常见的八种物质,它们之间的关系如图所示.A、C、F是氧化物,B是密度最小的气体,D是当前年产量最高的金属单质,F为植物光合作用的原料之一(图中“--“表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.).
A~H是初中化学常见的八种物质,它们之间的关系如图所示.A、C、F是氧化物,B是密度最小的气体,D是当前年产量最高的金属单质,F为植物光合作用的原料之一(图中“--“表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.).