题目内容
15.根据所学的科学知识,判断下列做法正确的是( )| A. | 实验室制气体时,先装药品再检查装置气密性 | |
| B. | 深夜醒来闻到浓烈煤气味时,应立即开灯检查家中煤气开关是否关闭 | |
| C. | 水和无机盐在导管内自下而上运输主要是因为蒸腾作用产生的拉力作用 | |
| D. | 高层住宅起火时应先用毛巾蒙鼻,再匍匐前进快速寻找电梯撤离,不可盲目跳楼 |
分析 A、实验室制取气体时,组装好装置后,应在向容器中装入药品前检查装置气密性.
B、煤气与空气或与氧气混合达到一定程度时遇明火会发生爆炸,来分析.
C、蒸腾作用是水分从活的植物体内以水蒸气的状态散失到大气中的过程,植物的蒸腾作用散失的水分约占植物吸收水的99%.
D、根据楼房着火会停电分析;
解答 解:A、实验室制取气体时,组装好装置后,应在向容器中装入药品前检查装置气密性,然后再装入药品,以避免装入药品后发现装置气密性不好,更换部分仪器而浪费药品;故选项说法错误.
B、煤气与空气或与氧气混合达到一定程度时遇明火会发生爆炸,若晚上发现家中煤气泄漏,不能做的事情是不能开电灯或打电话或使用打火机.所以错误.
C、蒸腾作用产生的蒸腾拉力,促进了植物对水分和无机盐的吸收与运输,故正确.
D、楼房着火会很快停电,乘电梯逃生会被困在电梯中,故做法错误;
故答案为:C
点评 要想解答好这类题目,要理解和熟记安全事故的原因及解决的科学方法,以及与之相关的知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2. 如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.下列说法正确的是( )
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.下列说法正确的是( )
 如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.下列说法正确的是( )
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.下列说法正确的是( )| A. | t1℃时甲、丙物质溶液中溶质质量分数一定相等 | |
| B. | 将t2℃时甲、乙、丙三种物质的饱和溶液分别降温至t1℃,所得溶液的溶质质量分数:乙>甲>丙 | |
| C. | t2℃时甲、乙、丙的饱和溶液分别恒温蒸发等量的水,析出溶质的质量:甲>乙>丙 | |
| D. | 若使点a的甲溶液60g,转化到点b,至少应加入30g甲固体 |
6.同学们运用对比的学习方法探究碱的性质.
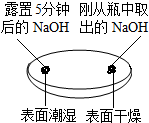
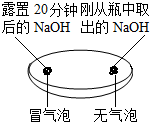
(1)由实验一、二可知,氢氧化钠会吸收空气的H2O、CO2,因此要密封保存.
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,对比A瓶与C(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙两种饱和溶液.
(4)某同学发现工业上使用的氢氧化钠固体标签如图所示,于是对其成分进行了探究:

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】
①在化工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\stackrel{通电}{→}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过量稀盐酸
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中的氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
| 实验一 观察固体表面 | 实验二 向两块固体表面滴加稀盐酸 | 实验三 振荡3个塑料瓶 |
 |  | 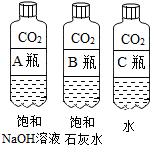 |
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,对比A瓶与C(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙两种饱和溶液.
| 实验一 | 实验二 | 分析 |
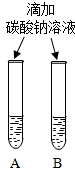 | 微热(不考虑水分蒸发)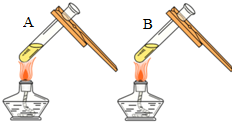 | 两种方案中均观察到A试管内出现白色浑浊,则A中溶液为饱和氢氧化钙溶液;;方案二的设计原理是氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大. |

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】
①在化工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\stackrel{通电}{→}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过量稀盐酸
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中的氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
20.取4份等质量的KClO3,向其中3份中分别加入少量等质量的KMnO4、MnO2和Mn,分别在某温度下加热至质量不再改变,测定产生氧气的质量.然后将剩余固体溶于足量水中,添加过少量物质的组别中均有相同组成的不溶物.测定结果如表:
已知ml>m2>m3,下列关于此实验的说法一定正确的是( )
| 组别 | ① | ② | ③ | ④ |
| 加入物质 | 无 | KMnO4 | MnO2 | Mn |
| 产生氧气的质量/g | 0 | ml | m2 | m3 |
| 不溶物的质量/g | 0 | wl | w2 | w3 |
| A. | 残留不溶性物质的质量关系为w1>w2>w3 | |
| B. | 不加入其他物质时,KClO3未发生分解反应 | |
| C. | KMnO4是KClO3分解制氧气效果最好的催化剂 | |
| D. | 3种物质的加入都有利于KClO3分解制氧气 |
4.仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是( )
| 选项 | A | B | C | D |
| 实验项目 | 除去KCl中少量的MnO2 | 用10mol/L的盐酸配制100mL0.1mol/L的盐酸 | 用氯化钠溶液制备氯化钠晶体 | 除去CO2气体中的HCl |
| 实验仪器 或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 | 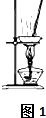 | 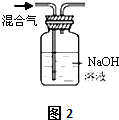 |
| A. | A | B. | B | C. | C | D. | D |
5.分子、原子和离子是构成物质的基本微粒.下列说法正确的是( )
| A. | 构成分子的原子能保持该物质的化学性质 | |
| B. | 原子得失电子变成离子后,元素的种类发生了变化 | |
| C. | 两种原子的质量之比等于它们的相对原子质量之比 | |
| D. | 离子之间存在着相互作用,分子间没有相互作用 |