题目内容
3.在一个密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表:| 物质 | A | B | C | D |
| 反应前质量(g) | 11 | 2 | 22 | 1 |
| 反应后质量(g) | x | 2 | 8 | 19 |
| A. | 参加反应的C与D质量比为22:1 | B. | x的值是4 | ||
| C. | B是该反应的催化剂 | D. | 该反应属于化合反应 |
分析 根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物.由表格信息可知11g+2g+22g+1g=X+2g+8g+19g,反应后X质量为7克,A质量减少是反应物;C质量减少了也是反应物;B质量不变,可能做催化剂,D质量增加的是生成物,符合“多变一”的特点,是化合反应,根据质量关系即可推出一些量之间的关系.
解答 解:根据质量守恒定律和表格信息可知:11g+2g+22g+1g=X+2g+8g+19g,反应后X值为7克,A质量减少是反应物;C质量减少了也是反应物;B质量不变,可能做催化剂,D质量增加的是生成物,符合“多变一”的特点,是化合反应.
A、参加反应的C与D质量比为:14:18=7:9,错误;
B、反应后X值为7,错误;
C、B质量不变,可能做催化剂,错误;
D、由分析可知,该反应是化合反应,正确.
故选D.
点评 解此题需根据质量守恒定律,认真分析各物质的质量变化情况,仔细推敲,即可求解.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
11.下列物质在氧气中燃烧,无火焰产生的是( )
| A. | 硫 | B. | 蜡烛 | C. | 氢气 | D. | 铁丝 |
8.下列除杂设计正确的是( )
| 序号 | 物 质 | 杂 质 | 所用试剂或方法 |
| A | CaCl2溶液 | 盐酸 | 过量CaCO3,过滤 |
| B | MnO2 | KCl | 溶解,过滤,蒸发 |
| C | KClO3 | KCl | 加热至不再产生气体 |
| D | CuSO4溶液 | FeSO4 | 加入足量铁粉,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
15.如图为四种粒子的结构示意图,以下对相关粒子的描述不正确的是( )
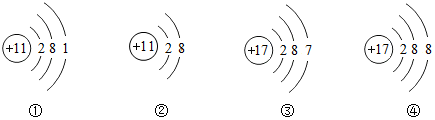

| A. | ②④具有相对稳定结构 | B. | ①②属于同种元素 | ||
| C. | ②④形成的化合物为NaCl | D. | ①③都容易失去电子 |
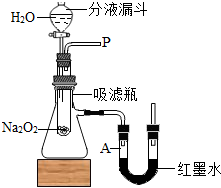 某化学兴趣小组的同学,利用如图装置和药品进行探究.他们设计的探究过程如下:
某化学兴趣小组的同学,利用如图装置和药品进行探究.他们设计的探究过程如下: