题目内容
2.发射卫星的火箭用联氨(N2H4)作燃料,用四氧化二氮(N204)作助燃剂,反应的化学方程式为:2N2H4+N2O4$\frac{\underline{\;点燃\;}}{\;}$3N2+4H2O,生成物不污染空气,低碳环保.请计算3.2kgN2H4完全燃烧后生成N2的质量.分析 根据反应的化学方程式和提供的数据可以计算3.2kgN2H4完全燃烧后生成N2的质量.
解答 解:设生成氮气的质量为x,
2N2H4+N2O4$\frac{\underline{\;点燃\;}}{\;}$3N2+4H2O,
64 84
3.2kg x
$\frac{64}{3.2kg}$=$\frac{84}{x}$,
x=4.2kg,
答:3.2kgN2H4完全燃烧后生成N2的质量是4.2kg.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
13.硫酸亚铁铵晶体俗名为莫尔盐,是一种蓝绿色的无机复盐,化学式为(NH4)2Fe(SO4)2•6H2O,在医药、电镀方面有广泛的应用.某化学兴趣小组的学生打算用含有少量铜的废铁屑来制取硫酸亚铁铵晶体.(硫酸亚铁铵晶体易溶于水,不溶于乙醇;硫酸亚铁铵晶体在100℃-110℃时分解)(反应涉及到三种盐的溶解度见附表)
制备流程如图所示:
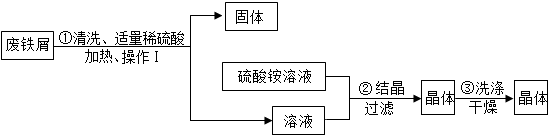
(1)废铁屑倒入容器中,倒入热水和洗涤剂,充分搅拌.目的是利用洗涤剂的乳化作用,除去铁屑表面的油污.
(2)操作I要趁热进行的原因是防止硫酸亚铁以晶体形式沉降,得到的固体中一定含有的物质是铜.
(3)当通过浓缩硫酸亚铁与硫酸铵混合液时,能得到硫酸亚铁铵晶体.步骤②适宜用降温结晶法.
(4)洗涤干燥时,有人建议使用无水酒精洗涤快速晾干.这样的优点是AB(填序号).
A.避免用水洗涤所造成的晶体损耗
B.酒精挥发能带走水分,无需烘干,避免强热烘干造成晶体分解.
| 附表 三种盐的溶解度(/g) | |||
| 温度/℃ | FeSO4 | (NH4)2SO4 | (NH4)2Fe(SO4)2•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |

(1)废铁屑倒入容器中,倒入热水和洗涤剂,充分搅拌.目的是利用洗涤剂的乳化作用,除去铁屑表面的油污.
(2)操作I要趁热进行的原因是防止硫酸亚铁以晶体形式沉降,得到的固体中一定含有的物质是铜.
(3)当通过浓缩硫酸亚铁与硫酸铵混合液时,能得到硫酸亚铁铵晶体.步骤②适宜用降温结晶法.
(4)洗涤干燥时,有人建议使用无水酒精洗涤快速晾干.这样的优点是AB(填序号).
A.避免用水洗涤所造成的晶体损耗
B.酒精挥发能带走水分,无需烘干,避免强热烘干造成晶体分解.
10. 2015年2月,医用氧气袋(如图)首次获准带上火车,对于一些特殊的患者非常重要.下列有关医用氧气的说法和做法中不正确的是( )
2015年2月,医用氧气袋(如图)首次获准带上火车,对于一些特殊的患者非常重要.下列有关医用氧气的说法和做法中不正确的是( )
 2015年2月,医用氧气袋(如图)首次获准带上火车,对于一些特殊的患者非常重要.下列有关医用氧气的说法和做法中不正确的是( )
2015年2月,医用氧气袋(如图)首次获准带上火车,对于一些特殊的患者非常重要.下列有关医用氧气的说法和做法中不正确的是( )| A. | 医用氧气袋要采用柔软的橡皮密封 | |
| B. | 医用氧气可用工业制氧方法,发生了化学变化 | |
| C. | 缺氧性患者在疾病发作时才可用氧气袋吸氧 | |
| D. | 携带医用氧气袋时要避开烟头等明火 |
17.我国纪念2015年“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.以下不符合这一主题的做法是( )
| A. | 工业废水直接排放到河流中 | B. | 禁止使用含磷洗衣粉 | ||
| C. | 合理使用农药化肥 | D. | 淘米水用于浇花 |
14.分类是学习化学的重要方法之一.下列说法中正确的是( )
| A. | 不锈钢、金刚石和黄铜属于合金 | |
| B. | 硝酸铵、尿素和氯化铵属于氮肥 | |
| C. | 液氧、盐酸和石灰水属于混合物 | |
| D. | 塑料、涤纶、棉花属于有机高分子合成材料 |
16. 同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
(1)探究成分
①小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是一定不是NaCl溶液(可能是NaOH,Na2CO3或NaOH和Na2CO3的混合溶液).他取少量待测液于试管中,加入过量的稀HCl,看到有气泡产生,由此小张同学认为,溶液为Na2CO3溶液.
②小李同学对小张同学的结论提出疑问,拟进行了以下实验:取少量待测液于试管中,加入过量的BaCl2溶液,生成白色沉淀,该反应方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl,过滤,取滤液,(写出还需进行的操作及现象)滴加无色酚酞溶液,溶液变红色或滴加硫酸铜溶液,产生蓝色沉淀(合理即可).通过实验,小李认为小张结论不正确.
③同学们通过讨论认为试剂瓶原标签应该是氢氧化钠,但因吸收空气中CO2的而变质.
(2)测定碳酸钠的浓度
取该试剂瓶中溶液50g倒入烧杯中,再向烧杯中逐滴滴加盐酸使其充分反应至无气泡产生(假设生成的二氧化碳全部逸出).测得加入盐酸的质量与烧杯中的物质的质量关系如表所示.
请你计算:
①这一测定过程中产生二氧化碳质量为2.2g.
②这一瓶试剂中碳酸钠的质量分数(写出计算过程).
 同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:(1)探究成分
①小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是一定不是NaCl溶液(可能是NaOH,Na2CO3或NaOH和Na2CO3的混合溶液).他取少量待测液于试管中,加入过量的稀HCl,看到有气泡产生,由此小张同学认为,溶液为Na2CO3溶液.
②小李同学对小张同学的结论提出疑问,拟进行了以下实验:取少量待测液于试管中,加入过量的BaCl2溶液,生成白色沉淀,该反应方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl,过滤,取滤液,(写出还需进行的操作及现象)滴加无色酚酞溶液,溶液变红色或滴加硫酸铜溶液,产生蓝色沉淀(合理即可).通过实验,小李认为小张结论不正确.
③同学们通过讨论认为试剂瓶原标签应该是氢氧化钠,但因吸收空气中CO2的而变质.
(2)测定碳酸钠的浓度
取该试剂瓶中溶液50g倒入烧杯中,再向烧杯中逐滴滴加盐酸使其充分反应至无气泡产生(假设生成的二氧化碳全部逸出).测得加入盐酸的质量与烧杯中的物质的质量关系如表所示.
| 累计加入盐酸的质量/g | 0 | 25 | 37.5 | 50 |
| 烧杯中物质的总质量/g | 50 | 75 | 85.3 | 97.8 |
①这一测定过程中产生二氧化碳质量为2.2g.
②这一瓶试剂中碳酸钠的质量分数(写出计算过程).