题目内容
17.如图所示的实验操作中正确的是( )| A. | 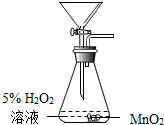 制取O2 制取O2 | B. | 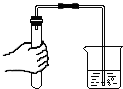 检查装置的气密性 检查装置的气密性 | ||
| C. | 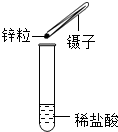 加入药品 加入药品 | D. | 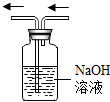 除去CO中的CO2 除去CO中的CO2 |
分析 A、根据实验室制取氧气的注意事项,进行分析判断.
B、根据检查装置气密性的方法进行分析判断.
C、根据向试管中装块状或颗粒状固体药品的方法进行分析判断.
D、图中装置起洗气功能时进气管与出气管的方向是“长进短出”.
解答 解:A、实验室制取氧气时,为防止生成的氧气从漏斗中逸出,漏斗的末端应伸入液面以下,图中所示装置错误.
B、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确.
C、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在试管口,再慢慢将试管竖立起来;应先加入固体,再加入液体,图中所示操作错误.
D、二氧化碳能与氢氧化钠溶液反应,一氧化碳不能,但图中装置起洗气功能时进气管与出气管的方向是“长进短出”,图中进气管与出气管的方向错误,图中所示装置错误.
故选:B.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
7.检验集气瓶中是否充满氧气的方法是( )
| A. | 将带火星的木条伸入集气瓶内 | B. | 将燃着的木条伸入集气瓶内 | ||
| C. | 将带火星的木条放在集气瓶口 | D. | 闻氧气的气味 |
5.在托盘天平两边各放一只烧杯,调至平衡.在烧杯里分别注入质量相同、溶质质量分数也相同的稀硫酸,若向右盘烧杯投入一定质量的镁,恰好完全反应,为使天平仍保持平衡,应向左盘烧杯里投入与镁质量相同的纯净金属是( )
| A. | Fe | B. | Al | C. | Zn | D. | Ag |
12.海水主要含有NaCl、MgCl2等物质,目前世界上60%的镁是从海水中提取的.小红同学模拟以下化工厂生产流程,以海水和贝壳(主要成分是碳酸钙)为原料来制取生产镁的原料----无水MgCl2.
(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
(2)除杂过程
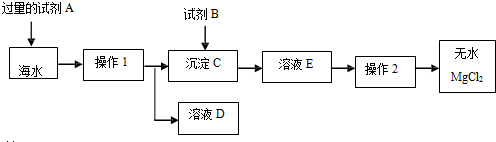
①在30℃;试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器.除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g 的Mg.
(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
| 温度(℃) 溶解度(g) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 氢氧化钠 | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 |
| 氢氧化钙 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 | 0.105 | 0.095 | 0.08 |

①在30℃;试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器.除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g 的Mg.
9.到1990年,人类已知结构的化学物质是1000万种,2009年9月8日为5000万种.2011年5月23日中国医学科学院药物研究所研究人员发现了一种新物质,并向中国专利技术局申请了专利,该物质被CAS登记为第6000万种已知结构的新物质M(化学式为C19H15N4FSO2).下列说法错误的是( )
| A. | M由六种元素组成,属于化合物 | B. | M的相对分子质量是42 | ||
| C. | M中氮氧原子个数比为2:1 | D. | M中碳元素的质量分数最大 |
6. 如图是某科技馆的一台“永动机”,由5根轻杆和转轴构成,轻杆的末端装有形状记忆合金制成的叶片,叶片进入热水后因伸展“划水”而转动,叶片离开热水后叶片形状迅速复原.关于该“永动机”的说法正确的是( )
如图是某科技馆的一台“永动机”,由5根轻杆和转轴构成,轻杆的末端装有形状记忆合金制成的叶片,叶片进入热水后因伸展“划水”而转动,叶片离开热水后叶片形状迅速复原.关于该“永动机”的说法正确的是( )
 如图是某科技馆的一台“永动机”,由5根轻杆和转轴构成,轻杆的末端装有形状记忆合金制成的叶片,叶片进入热水后因伸展“划水”而转动,叶片离开热水后叶片形状迅速复原.关于该“永动机”的说法正确的是( )
如图是某科技馆的一台“永动机”,由5根轻杆和转轴构成,轻杆的末端装有形状记忆合金制成的叶片,叶片进入热水后因伸展“划水”而转动,叶片离开热水后叶片形状迅速复原.关于该“永动机”的说法正确的是( )| A. | 随着科技的发展,人们可以制造出永动机 | |
| B. | 转动会使水温升得更高 | |
| C. | 记忆合金是一种新型化合物 | |
| D. | 水的内能转化为转轮的机械能 |
 A~H是初中化学教材中常见的8种物质,它们有如图所示的转化关系,已知A、C是无色液体,B、E、F、G、H是无色气体且F、G组成元素相同,其中D是黑色固体单质,E由两种元素组成,可在B中燃烧,且两种元素质量比为3:1.
A~H是初中化学教材中常见的8种物质,它们有如图所示的转化关系,已知A、C是无色液体,B、E、F、G、H是无色气体且F、G组成元素相同,其中D是黑色固体单质,E由两种元素组成,可在B中燃烧,且两种元素质量比为3:1.