题目内容
12.海水主要含有NaCl、MgCl2等物质,目前世界上60%的镁是从海水中提取的.小红同学模拟以下化工厂生产流程,以海水和贝壳(主要成分是碳酸钙)为原料来制取生产镁的原料----无水MgCl2.(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
| 温度(℃) 溶解度(g) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 氢氧化钠 | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 |
| 氢氧化钙 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 | 0.105 | 0.095 | 0.08 |
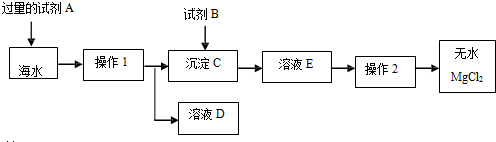
①在30℃;试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器.除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g 的Mg.
分析 经过操作I后出现了沉淀和溶液,而所有的钠的化合物都溶于水,只能是镁离子的沉淀,根据贝壳的主要成分是碳酸钙,碳酸钙在高温的条件下产生的氧化钙和水会生成氢氧化钙,结合这些知识书写方程式.根据过滤除了所给的仪器外,还需要倾倒液体的装置和盛放滤液的装置进行分析,根据试剂B是用来溶解沉淀C的,以及最后得到的氯化镁进行分析,根据元素的相对原子质量进行计算,根据氯化镁中镁元素的质量分数进行计算.
解答 解:①在30℃时,氢氧化钠的溶解度大于氢氧化钙,故最好选用氢氧化钠,氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,
故填:NaOH;MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
②除了题中给出的仪器之外,还需要有倾倒液体的装置和盛放滤液的装置,
故填:烧杯;
③经过操作I后将氢氧化镁分离了出来,而后面需要得到无水氯化镁,所以加入的试剂B就是为了生成氯化镁,需要加入盐酸,
故填:Mg(OH)2+2HCl=MgCl2+2H2O;
④镁的相对原子质量是24,氯的相对原子质量是35.5,所以MgCl2的相对分子质量=24+35.5×2=95,
设质量为x的氯化镁中含有镁元素的质量为12g,则有:x×$\frac{24}{95}$×100%=12g,x=47.5g,
故填:95,47.5.
点评 在解此类题时,首先要弄清楚生成流程中各个操作步骤的作用和所加试剂的作用,然后结合题中的问法逐一的解答.过滤操作可以将固体和液体进行分离.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列实验操作中不应该接触的是( )
| A. | 向试管中加入液体试剂时,试剂瓶口与试管 | |
| B. | 滴加试剂时,滴管与试管内壁 | |
| C. | 过滤时漏斗管口与烧杯内壁 | |
| D. | 过滤时盛待过滤液体的烧杯口与玻璃棒 |
3.下列变化前后的数据关系不符合a>b的是( )
| A. | 一瓶稀硫酸溶液的pH=a,将其加水稀释后溶液的pH=b | |
| B. | 一瓶浓盐酸的质量为a,敞口放置一段时间后质量为b | |
| C. | 一瓶浓硫酸溶质的质量分数为a,敞口放置一段时间后溶质质量分数为b | |
| D. | 酒精和水混合前的体积之和为a,混合后总体积为b |
17.如图所示的实验操作中正确的是( )
| A. | 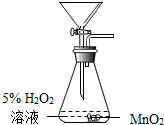 制取O2 制取O2 | B. | 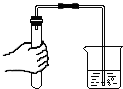 检查装置的气密性 检查装置的气密性 | ||
| C. | 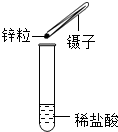 加入药品 加入药品 | D. | 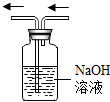 除去CO中的CO2 除去CO中的CO2 |
1.如今“低碳”生活方式已经悄然走进中国,一些可以计算个人排碳量的计算器在网上日益火爆.例如有一个“CO2排放量查询”的计算器,你只要任意输入飞机飞行公里数、汽车耗油公升数以及用电度数,你就可以简要地查出你的二氧化碳排量,然后屏幕还会提示你应该种上多少棵树才足够进行补偿.下列“低碳生活”的方式中,你认为不妥当的是( )
| A. | 提倡乘坐公共交通工具、骑自行车或步行的方式出行 | |
| B. | 广泛使用一次性筷子、一次性塑料袋 | |
| C. | 在生产和生活中提倡使用节能技术和节能用具 | |
| D. | 开发无污染的太阳能、风能、地热能等 |
 世界环境日的主题为:“水:20亿生命之所系”,请你参与下列问题的讨论.
世界环境日的主题为:“水:20亿生命之所系”,请你参与下列问题的讨论.