题目内容
7.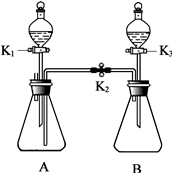 利用如图所示装置进行如下实验(装置气密性良好,实验前K1、K2、K3均处于关闭状态).
利用如图所示装置进行如下实验(装置气密性良好,实验前K1、K2、K3均处于关闭状态).(1)研究可燃物燃烧条件
若A装置的锥形瓶中放一小块白磷,白磷不燃烧.分液漏斗中放入80℃的热水,打开K1,使热水流入锥形瓶中浸没白磷,关闭K1,白磷仍不燃烧.打开K2、K3,待液体注入锥形瓶后关闭K3,观察到A中有气泡产生且白磷燃烧,则B中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,由此得出可燃物燃烧的条件是有氧气参加,温度达到可燃物的着火点.
(2)研究碱的性质
若A装置的锥形瓶中放入滴有酚酞的氢氧化钙溶液,分液漏斗中盛放足量的稀盐酸,B装置的锥形瓶中充满二氧化碳,分液漏斗中盛放一定量的氢氧化钠溶液.
①实验时,打开K1,滴入稀盐酸至A中溶液恰好变为无色,关闭K1,A中反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O.
②后续实验过程中观察到A中液体流入B中,B中溶液变红且变浑浊,产生该现象的实验操作是打开K3,待液体注入锥形瓶后关闭K3,使A中液体流入B中的原因是二氧化碳被氢氧化钠溶液吸收后,锥形瓶内气压减小.
分析 (1)可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可;
过氧化氢在二氧化锰催化作用下分解生成水和氧气;
(2)氢氧化钙和稀盐酸反应生成氯化钙和水;
二氧化碳能和氢氧化钠反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠.
解答 解:(1)分液漏斗中放入80℃的热水,打开K1,使热水流入锥形瓶中浸没白磷,关闭K1,白磷仍不燃烧,说明温度达到白磷的着火点时,没有氧气参加时也不能燃烧;
打开K2、K3,待液体注入锥形瓶后关闭K3,观察到A中有气泡产生且白磷燃烧,说明B中反应生成了氧气,进一步可知B中是过氧化氢分解生成氧气,过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,由此得出可燃物燃烧的条件是.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;.
(2)①A中氢氧化钙和稀盐酸反应生成氯化钙和水,反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O.
故填:Ca(OH)2+2HCl═CaCl2+2H2O.
②后续实验过程中观察到A中液体流入B中,B中溶液变红且变浑浊,是因为流入B中的溶液中含有氯化钙,能和B中的碳酸钠反应生成碳酸钙沉淀和氯化钠,产生该现象的实验操作是:打开K3,待液体注入锥形瓶后关闭K3;
使A中液体流入B中的原因是二氧化碳被氢氧化钠溶液吸收后,锥形瓶内气压减小.
故填:打开K3,待液体注入锥形瓶后关闭K3;二氧化碳被氢氧化钠溶液吸收后,锥形瓶内气压减小.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

| 序 号 | ① | ② | ③ | ④ |
| 物 质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
(2)若要测定纯碱溶液的酸碱度,选用下列选项中③.
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
(3)槟榔芋皮上含有一种碱性的物质--皂角素,沾上它会使皮肤奇痒难忍.你认为可选用下列①来涂抹止痒.
①食醋(含醋酸) ②熟石灰 ③纯碱.
| A. |  氢氧化钠溶液加水稀释 | |
| B. |  将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合 | |
| C. |  向HCl与Na2SO4混合溶液中加入Ba (OH) 2溶液 | |
| D. |  等质量、等质量分数的过氧化氢溶液分别制取氧气 |

 请根据图中的信息回答问题.
请根据图中的信息回答问题.