题目内容
15.运用学过的化学知识填空:(1)测定溶液的酸碱度最简便的方法是使用pH试纸.
(2)有失去标签的①氯化钠溶液、②氢氧化钠溶液、③硫酸铜溶液、④稀硫酸四种溶液.将它们一一鉴别出来的先后顺序是③②④①(填序号).
(3)选择除盐酸以外的试剂来检验露置在空气中的NaOH已经变质Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
用化学反应方程式解释氢氧化钠变质的原因:2NaOH+CO2═Na2CO3+H2O.
分析 根据测定溶液的酸碱度使用pH试纸、物质的性质以及氢氧化钠能与二氧化碳反应生成碳酸钠和水而变质的知识进行分析解答即可.
解答 解:(1)测定溶液的酸碱度使用的是pH试纸,故填:pH试纸;
(2)根据硫酸铜溶液为蓝色,首先将硫酸铜鉴别出来,然后将硫酸铜溶液与剩余的三种溶液混合,产生蓝色沉淀的是氢氧化钠,能将蓝色沉淀溶解掉的是硫酸,剩余的是氯化钠溶液,故填:③②④①;
(3)氢氧化钠能与二氧化碳反应生成碳酸钠和水而变质,检验氢氧化钠变质就是检验碳酸钠的存在,可以使用氢氧化钙溶液,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;2NaOH+CO2═Na2CO3+H2O.
点评 本题考查的是常见的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
10.汽油是现代交通工具的主要能源,汽油的主要成分辛烷(C8H18),下列有关说法正确的是( )
| A. | 汽油是纯净物 | B. | 辛烷中碳、氢质量之比为4:9 | ||
| C. | 辛烷的相对分子质量是114 | D. | 辛烷中碳的质量分数为15.8% |
20.下列四个图象,分别对应四种操作过程,其中正确的是( )
| A. | 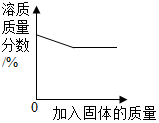 某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体 | |
| B. | 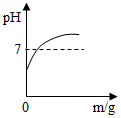 浓盐酸敞口放置 | |
| C. |  室温下向一定体积的NaOH溶液中加入稀盐酸 | |
| D. | 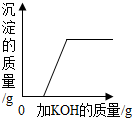 向HCl和CuCl2混合液中滴加KOH溶液 |
4.我国女科学家屠呦呦发现了青蒿素,一种用于治疗疟疾的药物,获得诺贝尔生理学或医学奖.关于青蒿素[C15H22O5]说法正确的是( )
| A. | 青蒿素属于氧化物 | B. | 青蒿素的相对分子质量是282g | ||
| C. | 青蒿素碳元素的质量分数最高 | D. | 青蒿素有42个原子 |
2.下列说法中,正确的是( )
| A. | 家用电器着火,立即用水泼灭 | |
| B. | 公路上的积雪可以用氯化钠来消除 | |
| C. | 发令枪中红磷燃烧时产生大量白雾 | |
| D. | 生铁和钢都是铁合金,在用途上没有区别 |

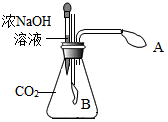 二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了图所示的实验装置(A、B是气球)探究二氧化碳与氢氧化钠溶液的反应.
二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了图所示的实验装置(A、B是气球)探究二氧化碳与氢氧化钠溶液的反应.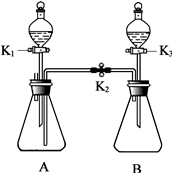 利用如图所示装置进行如下实验(装置气密性良好,实验前K1、K2、K3均处于关闭状态).
利用如图所示装置进行如下实验(装置气密性良好,实验前K1、K2、K3均处于关闭状态).