题目内容
19.如图所示的是几个常见的实验,请回答下列问题.
(1)实验甲中能观察到的明显现象是气球膨胀;
(2)通过实验乙可知水是由氢、氧元素组成,且二种元素的比例为1:8.
分析 氢氧化钠能和二氧化碳反应生成碳酸钠和水;
电解水生成氢气和氧气,根据水的化学式可以计算水中氢元素和氧元素质量比.
解答 解:(1)实验甲中,二氧化碳和氢氧化钠反应生成碳酸钠和水,瓶内气压减小,气球膨胀.
故填:气球膨胀.
(2)实验乙电解水生成氢气和氧气,由此可知水是由氢、氧元素组成,水的化学式是H2O,氢元素和氧元素质量比为:2:16=1:8.
故填:氢、氧;1:8.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.二氧化碳的过度排放会引起系列环境问题.某化学兴趣小组的同学设计了如下图的方法来吸收转化工业废气中的二氧化碳(部分产物已略).
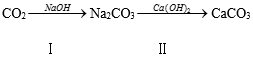
(1)下列环境问题与CO2有关的是B(填字母序号).
A.酸雨 B.温室效应 C.臭氧空洞 D.白色污染
(2)第Ⅰ步中不用价格更低的Ca(OH)2来直接吸收CO2的主要原因是Ca(OH)2微溶于水,吸收率低.
(3)第Ⅱ步反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(4)CaCO3在医疗上可用作补钙剂.
(5)已知部分原料的价格如下表所示.
上述工艺中,处理相同量的CO2,联合使用反应Ⅰ、Ⅱ比单用反应Ⅰ所需原料成本更低,原因是通过反应II实现了NaOH的循环利用,减少了NaOH的用量,所以成本降低.
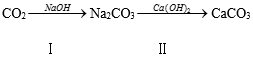
(1)下列环境问题与CO2有关的是B(填字母序号).
A.酸雨 B.温室效应 C.臭氧空洞 D.白色污染
(2)第Ⅰ步中不用价格更低的Ca(OH)2来直接吸收CO2的主要原因是Ca(OH)2微溶于水,吸收率低.
(3)第Ⅱ步反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(4)CaCO3在医疗上可用作补钙剂.
(5)已知部分原料的价格如下表所示.
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/Kg) | 0.36 | 2.90 |
4.我国女科学家屠呦呦发现了青蒿素,一种用于治疗疟疾的药物,获得诺贝尔生理学或医学奖.关于青蒿素[C15H22O5]说法正确的是( )
| A. | 青蒿素属于氧化物 | B. | 青蒿素的相对分子质量是282g | ||
| C. | 青蒿素碳元素的质量分数最高 | D. | 青蒿素有42个原子 |
5.某课外小组进行了如下实验.
(1)实验Ⅰ中反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)实验Ⅱ的目的是比较高锰酸钾和碘在汽油中的溶解情况.
(3)实验Ⅲ,倒流入集气瓶中的水小于瓶中气体体积的$\frac{1}{5}$,原因是红磷不足或气密性不好.
(4)实验Ⅳ中,观察到U型管左侧液面下降的原因是生石灰遇水放热,使得大试管中的气体受热膨胀,压强增大.
| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 实验 | 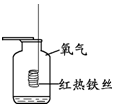 | 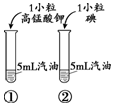 | 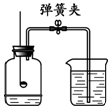 | 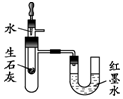 |
| 操作及现象 | 剧烈燃烧,火星四射,生成黑色固体,放热 | 试管①中固体几乎不溶解;试管②中固体溶解,形成紫红色溶液 | 红磷燃烧产生白烟,熄灭后冷却至室温,打开弹簧夹,水倒流入集气瓶中 | 将胶头滴管中的水滴入试管中,一段时间后,观察到U型管左侧液面下降 |
(2)实验Ⅱ的目的是比较高锰酸钾和碘在汽油中的溶解情况.
(3)实验Ⅲ,倒流入集气瓶中的水小于瓶中气体体积的$\frac{1}{5}$,原因是红磷不足或气密性不好.
(4)实验Ⅳ中,观察到U型管左侧液面下降的原因是生石灰遇水放热,使得大试管中的气体受热膨胀,压强增大.
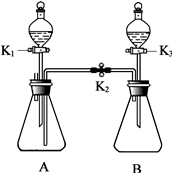 利用如图所示装置进行如下实验(装置气密性良好,实验前K1、K2、K3均处于关闭状态).
利用如图所示装置进行如下实验(装置气密性良好,实验前K1、K2、K3均处于关闭状态). 归纳总结是化学息息的常见方法,请根据所学知识回答问题:
归纳总结是化学息息的常见方法,请根据所学知识回答问题: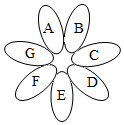 传说七瓣花可以帮你实现任何愿望.有A、B、C、D、E、F、G七种物质(如图),分别是铁、碳、氧气、二氧化碳、盐酸、熟石灰、纯碱中的一种,按照相邻花瓣的两种物质在一定条件下可以发生反应的原则,把它们拼成了美丽的七瓣花.已知A为非金属固体单质,C为其中一种化合物.请回答下列问题:
传说七瓣花可以帮你实现任何愿望.有A、B、C、D、E、F、G七种物质(如图),分别是铁、碳、氧气、二氧化碳、盐酸、熟石灰、纯碱中的一种,按照相邻花瓣的两种物质在一定条件下可以发生反应的原则,把它们拼成了美丽的七瓣花.已知A为非金属固体单质,C为其中一种化合物.请回答下列问题: