题目内容
请设计一个实验装置用以进行CO与CO2的分离和干燥,并简述其操作.
考点:混合物的分离方法,二氧化碳的化学性质
专题:物质的分离和提纯
分析:根据此题考查的是物质的分离.分离与除杂不同的是将物质分开后要恢复原状,要分离CO和CO2,由于CO一般不与液体物质反应,那么只能将CO2吸收之后再放出.
解答:解:CO2是酸性氧化物,可用碱来吸收使其生成碳酸盐,碳酸盐遇酸可放出CO2,所以甲中装有NaOH溶液,用来吸收CO2,此时从乙中出来的是被乙中浓硫酸干燥过的纯净的CO,因为该题中要求分离CO和CO2,所以最终还要求把甲中吸收的CO2再放出来,所以分液漏斗中装稀硫酸,用来生成CO2;故答案:
CO、CO2混合气体先通过装NaOH溶液的洗气瓶,再通过装浓H2SO4的洗气瓶,分离出干燥的CO2;然后再向吸收了CO2的装NaOH溶液的洗气瓶滴加足量的硫酸,使生成的CO再通过装浓H2SO4的洗气瓶,分离出干燥的CO2.

CO、CO2混合气体先通过装NaOH溶液的洗气瓶,再通过装浓H2SO4的洗气瓶,分离出干燥的CO2;然后再向吸收了CO2的装NaOH溶液的洗气瓶滴加足量的硫酸,使生成的CO再通过装浓H2SO4的洗气瓶,分离出干燥的CO2.
点评:做这类题时要注意看清要求,如:①除去CO中的CO2,②分离CO和CO2的混合物.是不一样的.

练习册系列答案
相关题目
向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,下列说法中正确的是( )
[提示:NaOH由Na+和OH-构成,NaOH溶于水时Na+和OH-分散到水分子之间].
[提示:NaOH由Na+和OH-构成,NaOH溶于水时Na+和OH-分散到水分子之间].
| A、溶液中的Na+总数不变 |
| B、单位体积内的OH-数目不变 |
| C、溶质的质量分数不变 |
| D、溶液的质量不变 |
有M、N和R三种金属,已知在它们的氧化物中只有N的氧化物溶于水,且其水溶液pH>7.M不溶于盐酸,R的盐不适宜在M质的容器中盛放.则M、N、R连同H四者在金属活动性顺序表中排列的先后顺序是( )
| A、N、M、H、R |
| B、R、H、M、N |
| C、R、M、H、N |
| D、N、H、M、R |
区别下列各组物质,所选择的试剂或方法错误的是( )
| A、空气与氧气一一带火星的木条 |
| B、氮气与二氧化碳气体一-燃着的木条 |
| C、水与澄清石灰水一一二氧化碳气体 |
| D、硬水与软水--肥皂水 |
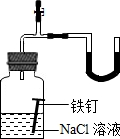



 利用如图所示的装置做物质导电性实验.
利用如图所示的装置做物质导电性实验.