题目内容
下列实验能达到目的是( )
| 实验 | 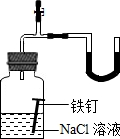 |
 |
 |
 |
| 目的 | 证明铁生锈过程 中空气参与反应 |
比较碳酸与硅酸的酸性强弱 | 制取BaSO3,并吸收尾气 | 吸收NH3 |
| 选项 | A | B | C | D |
| A、A | B、B | C、C | D、D |
考点:化学实验方案设计与评价,气体的净化(除杂),金属锈蚀的条件及其防护,酸的化学性质
专题:简单实验方案的设计与评价
分析:A、依据实验的现象推断解答;
B、依据强酸能够与弱酸盐反应生成弱酸分析解答;
C、依据两者反应的产物分析解答
D、依据氨气易溶于水,收集时要防止倒吸分析解答;
B、依据强酸能够与弱酸盐反应生成弱酸分析解答;
C、依据两者反应的产物分析解答
D、依据氨气易溶于水,收集时要防止倒吸分析解答;
解答:解:A.该铁钉能够生锈,现象为U形管左侧液面上升,右侧液面下降,可用于证明铁生锈过程中空气的某种成分参与反应,故A错误;
B.因为强酸能够与弱酸盐反应生成弱酸,所以盐酸能与碳酸钠反应生成的二氧化碳通入到硅酸钠的溶液中会置换出硅酸的沉淀,能证明碳酸比硅酸强,故B正确;
C.酸性条件下,硝酸根离子可氧化二氧化硫生成硫酸根离子,得到BaSO4沉淀,所以不能制取出BaSO3,故C错误;
D.氨气易与硫酸反应,不溶于CCl4,将氨气通入到CCl4,不会产生倒吸,故D正确;
故选B、D.
B.因为强酸能够与弱酸盐反应生成弱酸,所以盐酸能与碳酸钠反应生成的二氧化碳通入到硅酸钠的溶液中会置换出硅酸的沉淀,能证明碳酸比硅酸强,故B正确;
C.酸性条件下,硝酸根离子可氧化二氧化硫生成硫酸根离子,得到BaSO4沉淀,所以不能制取出BaSO3,故C错误;
D.氨气易与硫酸反应,不溶于CCl4,将氨气通入到CCl4,不会产生倒吸,故D正确;
故选B、D.
点评:本题考查化学实验方案的评价,涉及金属的腐蚀、非金属性的比较、物质的制备以及分离等探究实验,为高考常见题型,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握物质的性质的异同,难度不大.

练习册系列答案
相关题目
下列物质中属于有机高分子化合物的是( )
| A、酒精 | B、甲烷 | C、淀粉 | D、食醋 |
有400克硝酸钾的不饱和溶液分成两等份,在温度不变的情况下,一份蒸发掉60克水,析出3克晶体,另一份蒸发掉80克水,析出8克晶体.则该温度下硝酸钾的溶解度为( )
| A、5克 | B、10克 |
| C、20克 | D、25克 |
下列物质不属于合成材料的是( )
| A、腈纶 | B、尼龙 | C、塑料 | D、真丝 |