题目内容
9.把干燥、纯净的氯酸钾和二氧化锰的混合物15.2克装入大试管中加热制取氧气.待充分反应后,将试管冷却、称量,得到10.4克固体物质.计算:(1)制得氧气4.8克.
(2)7.4克固体物质中含有哪些物质?各多少克?
分析 加热氯酸钾和二氧化锰的混合物,氯酸钾受热分解生成氯化钾和氧气,二氧化锰在变化过程中为催化剂,反应前后质量和化学性质都不变;
(1)利用质量守恒定律,由反应前后固体物质的质量差,可求得放出气体氧气的质量;
(2)根据反应的化学方程式,利用生成氧气的质量可计算原混合物中氯酸钾的质量;
解答 解:(1)待反应至不再有气体生成后,制取氧气的质量=15.2g-10.4g=4.8g
设完全反应时生成氯化钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 4.8g
$\frac{149}{x}$=$\frac{96}{4.8g}$
x=7.45g
所以10.4克固体物质含有氯化钾质量为7.45g,二氧化锰质量为10.7g-7.45g=3.25g.
故答案为:(1)4.8;
(2)氯化钾质量为7.45g,二氧化锰质量为3.25g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
17.下列变化属于化学变化的是( )
| A. | 水结成冰 | B. | 人体呼吸 | C. | 酒精挥发 | D. | 电灯通电发光 |
14.下列有关原子结构的说法正确的是( )
| A. | 决定原子种类的粒子是原子核内的质子数 | |
| B. | 原子中的中子带负电荷 | |
| C. | 原子中质子与中子的数目一定相同 | |
| D. | 原子的质量主要集中在质子和电子上 |
1.根据如图进行实验(夹持仪器略去).实验过程:①通入N2,点燃酒精灯,加热一段时间使温度高于240℃;②熄灭酒精灯,立即改通O2.下列说法错误的是( )
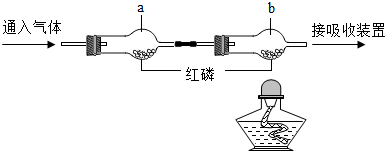

| A. | 实验过程①中,a、b中均无明显现象 | |
| B. | 实验过程②中,a中无现象,b中红磷燃烧 | |
| C. | 实验过程②中,对比a、b中的实验现象,可知可燃物燃烧的条件之一是温度要达到可燃物的着火点 | |
| D. | 实验过程①中,能说明可燃物燃烧的条件之一是与氧气接触 |
10.为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均错误的是( )
| 序号 | 样品成分 | 所选试剂 | 操作方法 |
| A | KCl(MnO2) | 水 | 溶解、过滤、蒸发结晶 |
| B | Na2CO3(NH4HCO3) | -- | 加热至质量不再减少 |
| C | NaCl(KNO3) | 水 | 热水溶解、趁热过滤 |
| D | NaCl(MgCl2) | 过量NaOH溶液 | 过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |


