题目内容
1.根据如图进行实验(夹持仪器略去).实验过程:①通入N2,点燃酒精灯,加热一段时间使温度高于240℃;②熄灭酒精灯,立即改通O2.下列说法错误的是( )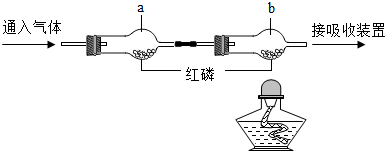
| A. | 实验过程①中,a、b中均无明显现象 | |
| B. | 实验过程②中,a中无现象,b中红磷燃烧 | |
| C. | 实验过程②中,对比a、b中的实验现象,可知可燃物燃烧的条件之一是温度要达到可燃物的着火点 | |
| D. | 实验过程①中,能说明可燃物燃烧的条件之一是与氧气接触 |
分析 根据燃烧的条件结合实验过程①②分析,注意变量的控制,选出正确的选项即可.
解答 解:A.在实验①中,a处的红磷温度没有达到其着火点,也没有与氧气接触,所以不能燃烧;b处的红磷是可燃物,温度达到着火点,但是通N2,氮气不能支持燃烧,所以此处的红磷不燃烧,说法正确;
B.实验②中a处的红磷虽然与氧气接触,但是温度没有达到其着火点,所以不能燃烧;b处的红磷既与氧气接触,温度又达到了其着火点,所以发生了燃烧,故说法正确;
C.实验②中b处的红磷是可燃物,温度达到着火点,然后通O2,燃烧,而a处没有燃烧,是温度没有达到着火点,说明可燃物燃烧需要温度达到着火点,故说法正确;
D.实验①中b通N2,不燃烧;实验②中b通O2,能燃烧,说明可燃物燃烧需要氧气,故说法错误.
故选D.
点评 通过回答本题知道了验证可燃物燃烧的条件的实验的设计过程.掌握了可燃物燃烧的条件.要会根据物质燃烧需要的三个条件去分析具体的实验现象.特别注意物质燃烧所需的三个条件缺一不可.

练习册系列答案
相关题目
12.我们通过对水的生成和分解实验的研究,认识了水的组成.水是由( )
| A. | 氢气和氧气组成的 | B. | 两个氢原子和一个氧原子构成的 | ||
| C. | 氢元素和氧元素组成的 | D. | 两个氢元素和一个氧元素组成的 |
16.“珍惜水,爱护水”是每个公民的责任和义务.下列说法正确的是( )
| A. | 淡水资源取之不尽,无需节约 | B. | 农作物采用大水漫灌 | ||
| C. | 大量使用农药、化肥 | D. | 加强对水资源的监测 |
13.下列标识与消防安全无关的是( )
| A. |  | B. |  | C. |  | D. |  |
1.为减少温室气体的排放,人们积极寻找不含碳元素的燃料.经研究发现,氨气燃烧产物没有污染,且释放大量能量,其微观示意图如图所示.下列说法错误的是( )
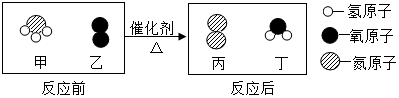

| A. | “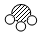 ”能保持氨气的化学性质 ”能保持氨气的化学性质 | B. | 该反应为置换反应 | ||
| C. | 生成物的分子个数比为1:1 | D. | 氧元素的化合价发生了变化 |
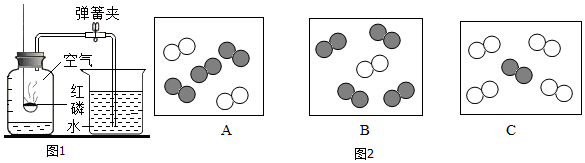
 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子.
”表示氧原子. ”可表示的微粒是氮分子(填名称).
”可表示的微粒是氮分子(填名称).