题目内容
18.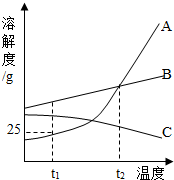 如图是A、B、C三种固体物质在水中的溶解度曲线,据图回答:
如图是A、B、C三种固体物质在水中的溶解度曲线,据图回答:(1)t1℃时A的饱和溶液80g,其中A的质量为16g;
(2)当A物质中混有少量B物质时,通常可采用降温结晶的方法提纯A,原因是A的溶解度受温度的影响比较大;
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂量不变),三种溶液中溶质的质量分数由大到小的顺序是B>C>A(填序号).
分析 根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;t1℃时,A的溶解度是25g,质量分数=$\frac{25g}{125g}×100%=20%$,A的饱和溶液80g,其中A的质量=80g×20%=16g;当A物质中混有少量B物质时,通常可采用降温结晶的方法提纯A,原因是A的溶解度受温度的影响比较大;将t1℃时,A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂量不变),三种溶液中溶质的质量分数由大到小的顺序是:B>C>A.
解答 解:(1)t1℃时,A的溶解度是25g,质量分数=$\frac{25g}{125g}×100%=20%$,A的饱和溶液80g,其中A的质量=80g×20%=16g;故答案为:16g;
(2)当A物质中混有少量B物质时,通常可采用降温结晶的方法提纯A,原因是A的溶解度受温度的影响比较大;故答案为:降温结晶;A的溶解度受温度的影响比较大;
(3)将t1℃时,A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂量不变),三种溶液中溶质的质量分数由大到小的顺序是:B>C>A;故答案为:B>C>A
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
9.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 叙述Ⅰ | 叙述Ⅱ | |
| A | 二氧化碳能与水反应生成碳酸 | 正常雨水显酸性,称为酸雨 |
| B | 电解水生成氢气和氧气 | 水由氢元素和氧元素组成 |
| C | 分子在不断的运动 | 5mL水和5mL酒精混合后小于10mL |
| D | 酸可与碱发生中和反应 | 用氢氧化钠改良酸性土壤 |
| A. | A | B. | B | C. | C | D. | D |
6.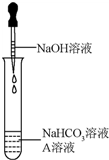 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$NaCO3+H2O+CO2↑
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
(1)写出上表格中Ⅰ的现象:有气泡产生; 写出上表格中Ⅱ所涉及到的化学方程式:Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
(2)实验过程:[实验1]证明反应生成了Na2CO3同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2. 有同学提出这个实验不足以证明有Na2CO3生成,其理由是_CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
[实验2]证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$NaCO3+H2O+CO2↑
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)实验过程:[实验1]证明反应生成了Na2CO3同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2. 有同学提出这个实验不足以证明有Na2CO3生成,其理由是_CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
[实验2]证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.
7.下列依据实验目的进行的实验设计,合理的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 从空气中获取纯净的氮气 | 用硫燃烧除去空气中的氧气 |
| B | 检验某物质中是否含有SO42- | 取样溶解,滴加BaCl2溶液和稀硝酸 |
| C | 除去混在氨气中的水蒸气 | 把混合气体通过足量的浓硫酸 |
| D | 鉴别硝酸铵和氯化钠固体 | 加适量的水溶解,测量前后温度变化 |
| A. | A | B. | B | C. | C | D. | D |
8.下列制取气体所用物质和装置均正确的是( )
| A. |  制取CO2 | B. |  制取氢气 | ||
| C. | 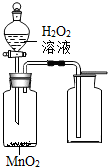 制取氧气 | D. |  制取氧气 |
 “低碳生活,绿色出行”.如图为潍坊公共自行车.请回答下列问题:
“低碳生活,绿色出行”.如图为潍坊公共自行车.请回答下列问题: