题目内容
8.碳酸的化学式为[H2CO3]试求:[相对原子质量:H:1,C:12,O:16](1)碳酸的相对分子质量为多少?
(2)碳酸中H,C,O 三种元素的质量比是?
(3)碳酸中氢的质量分数是多少?
(4)10克碳酸中氢的质量是多少?
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(4)根据一定质量的化合物中元素质量的计算方法来分析.
解答 解:(1)碳酸的相对分子质量为:1×2+12+16×3=62;故填:62;
(2)碳酸中H,C,O 三种元素的质量比:(1×2):12:(16×3)=1:6:24;故填:1:6:24;
(3)碳酸中氢元素的质量分数为:$\frac{1×2}{62}×100%$≈3.2%;故填:3.2%;
(4)10克碳酸中氢的质量:10g×3.2%=0.32g.故填:3.2g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
17.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 干冰 H2O | B. | 苏打 NaHCO3 | C. | 消石灰 CaO | D. | 火碱 NaOH |
15.下列含氮化合物中,氮元素化合价最低的是( )
| A. | NO | B. | NH3 | C. | HNO3 | D. | HNO2 |
13.如图是某化学反应的微观模拟示意图,下列说法错误的是( )


| A. | 反应前后原子种类、数目均不变 | |
| B. | 该反应中,反应物的分子数目比是1:2 | |
| C. | 该反应的化学方程式为CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O | |
| D. | 该反应是化合反应 |
20.下列关于相对原子质量的说法中,正确的是( )
| A. | 相对原子质量的单位都是克 | |
| B. | 与其他原子质量相比较的数值 | |
| C. | 一个原子的质量 | |
| D. | 与一种碳原子质量的1/12相比较所得的值 |

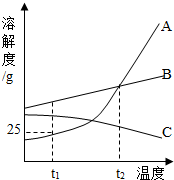 如图是A、B、C三种固体物质在水中的溶解度曲线,据图回答:
如图是A、B、C三种固体物质在水中的溶解度曲线,据图回答: