题目内容
7.CuCl2和MgCl2的混合溶液中加入过量锌粉,充分反应后过滤,留在滤纸上的物质是( )| A. | Zn | B. | Cu | C. | Zn、Cu | D. | Cu、Mg、Zn |
分析 锌的金属活动性比铜强,比镁弱,CuCl2和MgCl2的混合溶液中加入过量锌粉,锌能与氯化铜溶液反应生成氯化锌溶液和铜,不与氯化镁溶液反应,据此进行分析解答.
解答 解:锌的金属活动性比铜强,比镁弱,CuCl2和MgCl2的混合溶液中加入过量锌粉,锌能与氯化铜溶液反应生成氯化锌溶液和铜,不与氯化镁溶液反应,充分反应后过滤,留在滤纸上的物质是生成的铜和剩余的锌.
故选:C.
点评 本题难度不大,熟练掌握金属的化学性质、金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
相关题目
19.小红与妈妈做面包,发现妈妈揉面时加入了一种白色粉末,做出的面包疏松多孔,口感很好.她很感兴趣,想探究这种“神奇粉末”的成分.
【查阅资料】通过多市场上相关产品进行调查,小红发现了如图所示的三种商品.

其中,①快速发酵粉与水混合后,产生大量气体,你认为该气体是:CO2.
②纯碱和小苏打的性质如表.
小红妈妈告诉她所用的白色粉末就是以上三种商品中的一种.这种白色粉末是什么?
【设计实验】小红进行了如下实验:
(1)取少量白色粉末于试管中,加入适量蒸馏水,白色粉末溶解,无其他明显现象.说明白色粉末不是快速发酵粉.
(2)测得(1)中溶液的酸碱度,方法是:把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数,读得溶液pH≥10.
(3)取少量白色粉末于试管中,加入稀盐酸(或稀硫酸),有无色气体产生.根据上面的实验现象,小红认为白色粉末是纯碱.
【实验反思】你认为小红同学的结论正确吗?说明理由:不正确,因为碳酸氢钠也能产生相同的现象.
【知识拓展】若白色粉末为小苏打,则加热白色粉末后,根据产生的气体能使澄清石灰水变浑浊的现象,可以得到验证,加热白色粉末发生反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【查阅资料】通过多市场上相关产品进行调查,小红发现了如图所示的三种商品.

其中,①快速发酵粉与水混合后,产生大量气体,你认为该气体是:CO2.
②纯碱和小苏打的性质如表.
| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解时放热 | 20℃时溶解度9.8g,溶解时放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水 |
【设计实验】小红进行了如下实验:
(1)取少量白色粉末于试管中,加入适量蒸馏水,白色粉末溶解,无其他明显现象.说明白色粉末不是快速发酵粉.
(2)测得(1)中溶液的酸碱度,方法是:把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数,读得溶液pH≥10.
(3)取少量白色粉末于试管中,加入稀盐酸(或稀硫酸),有无色气体产生.根据上面的实验现象,小红认为白色粉末是纯碱.
【实验反思】你认为小红同学的结论正确吗?说明理由:不正确,因为碳酸氢钠也能产生相同的现象.
【知识拓展】若白色粉末为小苏打,则加热白色粉末后,根据产生的气体能使澄清石灰水变浑浊的现象,可以得到验证,加热白色粉末发生反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
17.如表是某同学探究金属活动性顺序的实验报告,请你在空白处填空.
| 实验步骤 | 实验现象 | 解释 |
| (1)将铁片、铜片分别投入到盛有稀盐酸的试管中. | 铁片的表面产生大量的气泡;铜片表面无现象; | 反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑ |
| (2)将铜片投入到盛有AgNO3溶液的试管中. | 在铜片的表面覆盖了一层银白色物质,溶液呈蓝色. | 反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 结论:Fe、Cu、Ag三种金属由强到弱的活动顺序为:Fe>Cu>Ag. | ||
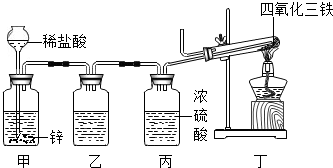 “引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃,如图所示是用新制的四氧化三铁与纯净、干燥的氢气制备“引火铁”的装置,请回答:
“引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃,如图所示是用新制的四氧化三铁与纯净、干燥的氢气制备“引火铁”的装置,请回答:


