题目内容
11.有一包固体粉末,可能由 CaCO3、CuSO4、Na2SO4、NaOH、KCl 五种物质中的两种或多种组成.为确定其组成,进行以下实验,请根据实验现象做出分析推理(设过程中所有发生的反应都恰好完全反应 ).Ⅰ.取一定质量的固体粉末,加适量水搅拌后过滤,得到沉淀 A 和无色溶液 B.
Ⅱ.向所得沉淀 A 中加入足量稀盐酸,得到无色气体和蓝色溶液.
III.取所得无色溶液 B 加入适量的 Ba(NO3)2溶液和足量稀硝酸,然后过滤,得白色沉淀 C 和无色溶液 D.
Ⅳ.取所得无色溶液 D 滴入适量 AgNO3溶液后又得白色沉淀 E 和无色溶液 F.
根据上述实验过程和发生的现象作出相应推理,填写以下空白:
(1)白色沉淀 E 的化学式是AgCl.
(2)无色溶液 F 中的溶质共有种,肯定存在的酸根离子为NO3-(写离子符号).
(3)写出步骤 III 中生成白色沉淀 C 的化学方程式是Ba(NO3)2+Na2SO4=2NaNO3+BaSO4↓.
(4)由实验过程及现象还不能.. 判断出该包粉末中含有的物质为Na2SO4(写化学式);得此结论的理由是步骤Ⅰ加水溶解时,混合物中的硫酸铜和氢氧化钠反应也能生成硫酸钠.
分析 根据碳酸钙难溶于水,CuSO4与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;而氢氧化铜与稀盐酸反应生成氯化铜溶液显蓝色,硫酸钠和Ba(NO3)2会生成不能溶于硝酸的白色硫酸钡沉淀,氯化钾与AgNO3溶液反应得白色沉淀氯化银和无色溶液硝酸钾,等知识进行分析.
解答 解:
根据碳酸钙难溶于水,CuSO4与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;而氢氧化铜与稀盐酸反应生成氯化铜溶液显蓝色,硫酸钠和Ba(NO3)2会生成不能溶于硝酸的白色硫酸钡沉淀,氯化钾与AgNO3溶液反应得白色沉淀氯化银和无色溶液硝酸钾,则:
(1)根据分析,白色沉淀E的化学式是AgCl.
(2)无色溶液F中的溶质共有3种:硝酸钠、硝酸钾、稀硝酸,肯定存在的酸根离子为NO3-.
(3)步骤Ⅲ中生成白色沉淀C的化学方程式Ba(NO3)2+Na2SO4=2NaNO3+BaSO4↓.
(4)由实验过程及现象还不能判断出该包粉末中含有的物质为Na2SO4;得出结论的理由是 步骤Ⅰ加水溶解时,混合物中的硫酸铜和氢氧化钠反应也能生成硫酸钠.
故答案为:
(1)AgCl.(2)3,NO3-.(3)Ba(NO3)2+Na2SO4=2NaNO3+BaSO4↓.
(4)Na2SO4;步骤Ⅰ加水溶解时,混合物中的硫酸铜和氢氧化钠反应也能生成硫酸钠.
点评 在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断,最后确定混合物的组成成分.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
1.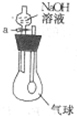 如图所示,在烧瓶里收集到某种气体,烧瓶用带导管(导管一端事先已绑好一个气球)的橡皮塞塞紧,当打开a处的活塞,加入浓NaOH溶液后,立即关闭活塞a,振荡,观察到气球迅速胀大,瓶中的气体可能是( )
如图所示,在烧瓶里收集到某种气体,烧瓶用带导管(导管一端事先已绑好一个气球)的橡皮塞塞紧,当打开a处的活塞,加入浓NaOH溶液后,立即关闭活塞a,振荡,观察到气球迅速胀大,瓶中的气体可能是( )
 如图所示,在烧瓶里收集到某种气体,烧瓶用带导管(导管一端事先已绑好一个气球)的橡皮塞塞紧,当打开a处的活塞,加入浓NaOH溶液后,立即关闭活塞a,振荡,观察到气球迅速胀大,瓶中的气体可能是( )
如图所示,在烧瓶里收集到某种气体,烧瓶用带导管(导管一端事先已绑好一个气球)的橡皮塞塞紧,当打开a处的活塞,加入浓NaOH溶液后,立即关闭活塞a,振荡,观察到气球迅速胀大,瓶中的气体可能是( )| A. | H2 | B. | SO2 | C. | O2 | D. | CO |
2.张老师在请同学说出“O2”表示的意义时,得到了以下几种回答,你认为正确的是( )
①表示氧气这种物质;②表示氧元素 ③表示2个氧原子 ④表示氧分子 ⑤表示1个氧分子里有2个氧原子 ⑥表示氧气是一种无色气体.
①表示氧气这种物质;②表示氧元素 ③表示2个氧原子 ④表示氧分子 ⑤表示1个氧分子里有2个氧原子 ⑥表示氧气是一种无色气体.
| A. | ③④⑤ | B. | ①④⑤⑥ | C. | ①③④⑤ | D. | ①④⑤ |
19.2015年7月29日,国家发改委召开河北省张家口市可再生能源示范区新闻通气会,会上宣布了《河北省张家口市可再生能源示范区发展规划》获国务院批复,同意设立张家口可再生能源示范区的消息.下列关于能源的说法中,正确的是( )
| A. | 天然气和可燃冰属于新能源 | B. | 风能和水能不会污染环境 | ||
| C. | 太阳能属于不可再生能源 | D. | 核能泄漏不会对人类产生危害 |
6.下列说法中有错误的是( )
| A. | 灭火方法--实验桌上少量酒精着火,用湿抹布盖灭 | |
| B. | 食品安全--亚硝酸钠对人体有害,不能食用 | |
| C. | 能源与环境--煤、石油、天然气等化石燃料燃烧后的产物对环境无影响 | |
| D. | 实验安全-稀释浓硫酸时要将浓硫酸沿烧杯壁慢慢注入水中并用玻璃棒不断搅拌 |
3.如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
①溶解度随温度升高而增大的物质是氢氧化钠.
②20℃时,Ca(OH)2的溶解度是0.14g.
③要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,其中措施不正确的是AB.(填序号)A.加入生石灰 B.升高温度 C.降低温度 D.恒温蒸发水
④20℃把90克NaOH投入到100克水中,配成溶液,其溶质的质量分数是47.4%.
⑤现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要除去Ca(OH)2,
应采取的物理方法是降温结晶并过滤.
⑥20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH靠近(填“靠近”或“偏离”)7.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 g/100g水 | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
②20℃时,Ca(OH)2的溶解度是0.14g.
③要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,其中措施不正确的是AB.(填序号)A.加入生石灰 B.升高温度 C.降低温度 D.恒温蒸发水
④20℃把90克NaOH投入到100克水中,配成溶液,其溶质的质量分数是47.4%.
⑤现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要除去Ca(OH)2,
应采取的物理方法是降温结晶并过滤.
⑥20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH靠近(填“靠近”或“偏离”)7.
7.CuCl2和MgCl2的混合溶液中加入过量锌粉,充分反应后过滤,留在滤纸上的物质是( )
| A. | Zn | B. | Cu | C. | Zn、Cu | D. | Cu、Mg、Zn |
8.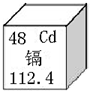 广西龙江河2012年1月15日出现重金属镉含量超标,1月26日污染水体进入下游柳江系统,给柳江流域造成了严重的水体污染,倍受社会各界关注.镉元素在元素周期表中的相关信息如图所示.下列说法中不正确的是( )
广西龙江河2012年1月15日出现重金属镉含量超标,1月26日污染水体进入下游柳江系统,给柳江流域造成了严重的水体污染,倍受社会各界关注.镉元素在元素周期表中的相关信息如图所示.下列说法中不正确的是( )
 广西龙江河2012年1月15日出现重金属镉含量超标,1月26日污染水体进入下游柳江系统,给柳江流域造成了严重的水体污染,倍受社会各界关注.镉元素在元素周期表中的相关信息如图所示.下列说法中不正确的是( )
广西龙江河2012年1月15日出现重金属镉含量超标,1月26日污染水体进入下游柳江系统,给柳江流域造成了严重的水体污染,倍受社会各界关注.镉元素在元素周期表中的相关信息如图所示.下列说法中不正确的是( )| A. | 镉原子核内有48个质子 | B. | 镉元素的原子序数是48 | ||
| C. | 镉原子的相对质量是112.4g | D. | 镉属于金属元素 |