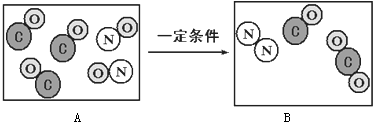
题目内容
15.现有碳、二氧化碳、水、锌、稀盐酸、氯化铜溶液、氢氧化钾溶液七种物质,请按下列要求写出相应的化学方程式.(每种物质不能重复使用)(1)有碳单质参与的化合反应CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO
(2)分解反应2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(3)实验室制取氢气的反应Zn+H2SO4═ZnSO4+H2↑
(4)有蓝色沉淀生成的反应2KOH+CuCl2=Cu(OH)2↓+2KCl.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)碳与二氧化碳在高温下反应生成一氧化碳,属于化合反应,反应的化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)水通电分解生成氢气和氧气,属于分解反应,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)实验室制取氢气,采用的是锌与稀硫酸反应,锌与稀硫酸反应生成硫酸锌溶液和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(4)氢氧化钾溶液与氯化铜溶液反应生成氢氧化铜沉淀和氯化钾,是有蓝色沉淀生成的反应,反应的化学方程式为:2KOH+CuCl2=Cu(OH)2↓+2KCl.
故答案为:(1)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;(3)Zn+H2SO4═ZnSO4+H2↑;(4)2KOH+CuCl2=Cu(OH)2↓+2KCl.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
19.2015年7月29日,国家发改委召开河北省张家口市可再生能源示范区新闻通气会,会上宣布了《河北省张家口市可再生能源示范区发展规划》获国务院批复,同意设立张家口可再生能源示范区的消息.下列关于能源的说法中,正确的是( )
| A. | 天然气和可燃冰属于新能源 | B. | 风能和水能不会污染环境 | ||
| C. | 太阳能属于不可再生能源 | D. | 核能泄漏不会对人类产生危害 |
3.如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
①溶解度随温度升高而增大的物质是氢氧化钠.
②20℃时,Ca(OH)2的溶解度是0.14g.
③要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,其中措施不正确的是AB.(填序号)A.加入生石灰 B.升高温度 C.降低温度 D.恒温蒸发水
④20℃把90克NaOH投入到100克水中,配成溶液,其溶质的质量分数是47.4%.
⑤现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要除去Ca(OH)2,
应采取的物理方法是降温结晶并过滤.
⑥20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH靠近(填“靠近”或“偏离”)7.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 g/100g水 | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
②20℃时,Ca(OH)2的溶解度是0.14g.
③要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,其中措施不正确的是AB.(填序号)A.加入生石灰 B.升高温度 C.降低温度 D.恒温蒸发水
④20℃把90克NaOH投入到100克水中,配成溶液,其溶质的质量分数是47.4%.
⑤现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要除去Ca(OH)2,
应采取的物理方法是降温结晶并过滤.
⑥20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH靠近(填“靠近”或“偏离”)7.
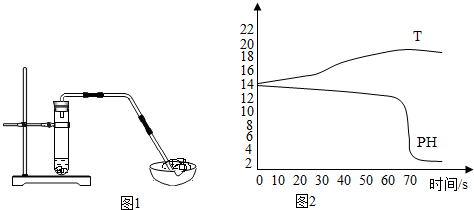
20.小明家面盆下水道堵上了,小明妈妈买了一盒“管道通”,按照说明放了一些在下水道管道中,一会儿,管道中出现“沸腾”,产生大量气体,堵塞的管道畅通了.小明很好奇,打开一盒“管道通”,内有一袋银灰色粉末和一袋白色颗粒.它们究竟是什么物质?于是进行了以下探究.
【查询资料】
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热.
(3)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道.
【猜想一】银灰色粉末为铝粉.
请你写出铝和稀盐酸反应的化学方程式:2Al+6HCl═2AlCl3+3H2↑.
【猜想二】白色颗粒为氢氧化钠.
【交流与反思】
图2是小明和老师一起向氢氧化钠溶液中逐渐滴入稀盐酸时用数字化实验测定的反应溶液温度和pH的变化曲线.氢氧化钠溶液与稀盐酸反应类型是中和反应;请你思考:
①为什么在0-60秒 pH变化不大?氢氧化钠溶液没反应完;
②请从曲线中找出该反应类型的两条规律:
该反应为放热反应;
两种物质恰好完全中和时,反应放热最大.

【查询资料】
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热.
(3)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道.
【猜想一】银灰色粉末为铝粉.
| 实验操作 | 实验现象 | 实验结论 |
| ①向如图1两套相同装置的试管中分别依次加入银灰色粉末和20mL稀盐酸;银灰色粉末和20mL氢氧化钠溶液 ②点燃气泡 | ①肥皂液产生无色气泡还漂浮起来 ②气泡可以(填可以/不可以)点燃,发生爆鸣声 | 银灰色粉末是铝粉 |
【猜想二】白色颗粒为氢氧化钠.
| 实验操作 | 实验现象 | 实验结论 |
| 将几粒白色固体颗粒放在表面皿上,放置一会儿;再将白色颗粒加入适量水,测pH;再向溶液中加几根头发,加热 | 固体表面潮湿并逐渐溶解 pH>7; 头发逐渐消失 | 白色固体为氢氧化钠 |
图2是小明和老师一起向氢氧化钠溶液中逐渐滴入稀盐酸时用数字化实验测定的反应溶液温度和pH的变化曲线.氢氧化钠溶液与稀盐酸反应类型是中和反应;请你思考:
①为什么在0-60秒 pH变化不大?氢氧化钠溶液没反应完;
②请从曲线中找出该反应类型的两条规律:
该反应为放热反应;
两种物质恰好完全中和时,反应放热最大.
7.CuCl2和MgCl2的混合溶液中加入过量锌粉,充分反应后过滤,留在滤纸上的物质是( )
| A. | Zn | B. | Cu | C. | Zn、Cu | D. | Cu、Mg、Zn |
5.如图是A和B在点燃的条件下反应生成C和D的微观示意图.据此判断下列说法正确的是( )
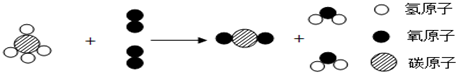

| A. | 有3种分子参加该反应 | |
| B. | 该反应属于分解反应 | |
| C. | 该反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | |
| D. | 该反应属于化合反应 |