题目内容
11.通过学习,我们已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,请结合如图回答问题
(1)写出图中标号仪器的名称:a分液漏斗;b集气瓶.
(2)当用装置C和D组合制取氧气时,实验结束后,应先操作A.
A.导气管从水槽中取出 B.熄灭酒精灯
(3)写出以C为发生装置来制取氧气的一个化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,若用装置D收集得到的氧气不纯,其原因可能是刚出现气泡就开始收集(写出1条即可).
(4)通过查阅资料得知:实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气(NH),氨气是一种密度比空气小,且极易溶于水的气体,其水溶液称为氨水.实验室制取氨气应选用的发生装置和收集装置是CF(填写字母编号)
分析 (1)依据实验室常用仪器的认识进行分析;
(2)根据实验室制取氧气时的注意事项分析回答;
(3)根据给试管中的固体加热及排水法收集氧气的注意事项分析回答;
(4)气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.
解答 解:(1)图中标号仪器的名称:a是分液漏斗;b是集气瓶;
故答案为:分液漏斗;集气瓶;
(2)当用装置C和D组合制取氧气时,实验结束后,应该先移出导管,再熄灭酒精灯,防止水倒流而炸裂试管;
故答案为:A;
(3)实验室常用加热高锰酸钾或氯酸钾的方法制氧气,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;用装置D收集得到的氧气不纯,其原因可能是:刚出现气泡就开始收集,收集前集气瓶中的水不满;
故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;刚出现气泡就开始收集;
(4)用加热氯化铵和氢氧化钙的固体混合物制取氨气,属于固体加热型,故选发生装置C,氨气的密度比空气小且极易溶于水,所以只能用向下排空气法收集;
故答案为:CF.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了仪器的名称、化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
2.下列各图所示的实验操作中,正确的( )
| A. |  检查装置的气密性 | B. |  点燃酒精灯 | ||
| C. |  制取氧气 | D. |  滴加溶液 |
19.从如图获取的信息中错误的是( )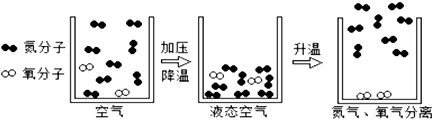

| A. | 空气是一种混合物 | B. | 氮气沸点比氧气低 | ||
| C. | 该过程为化学变化 | D. | 氧气由氧分子构成 |
3.目前,诺如病毒感染已经日趋严重,现在最有效的预防方法之一就是消毒液对空气消毒.84消毒液是含氯消毒液,主要成分为次氯酸钠,它能高效灭菌、无味.无毒、无腐化、无致敏反响,对诺如病毒的快速杀灭效果十分显著.已被广泛用于学校、机场等公共场所各类病毒沾染性的防疫.我校决定近期每天用次氯酸钠消毒液对全校教室、寝室全面消毒.小明观察到消毒液瓶上的标签如下表所示.
求:(1)这瓶1000毫升次氯酸钠消毒液的质量是1200克,其中含溶质次氯酸钠300克
(2)若将这种次氯酸钠消毒液500毫升与2400克水均匀混合,所得稀次氯酸钠消毒液中次氯酸钠的质量分数是多少?
(3)我校欲配制30千克质量分数为2%的稀次氯酸钠消毒液用来消毒,需要几瓶这样的消毒液?
| 消毒液1000毫升 | |
| 溶质的质量分数 | 25% |
| 密度 | 1.2克/厘米3 |
| 相对分子质量 | 74.5 |
| 腐蚀性;致敏性;游离氯可能引起中毒 | |
(2)若将这种次氯酸钠消毒液500毫升与2400克水均匀混合,所得稀次氯酸钠消毒液中次氯酸钠的质量分数是多少?
(3)我校欲配制30千克质量分数为2%的稀次氯酸钠消毒液用来消毒,需要几瓶这样的消毒液?
20.物质的分离方法很多,假如在食盐中混有下列杂质,你认为可以用过滤方法除去的是( )
| A. | 食盐中的蔗糖 | B. | 食盐中的沙石 | C. | 食盐中的红墨水 | D. | 食盐中的水 |
1.按要求完成下列表格:
| 物质名称(俗名) | 熟石灰 | 食盐 | |||
| 化学式 | NaOH | Na2CO3 | CaCO3 | ||
| 用途 | / | / |
 某化学兴趣小组的同学为测定石灰石样品中碳酸钙的含量(杂质不溶于水也不溶于酸),同学们取石灰石样品16克,放入68.4克盐酸中,恰好完全反应,测得物质总质量的变化如图所示,求:
某化学兴趣小组的同学为测定石灰石样品中碳酸钙的含量(杂质不溶于水也不溶于酸),同学们取石灰石样品16克,放入68.4克盐酸中,恰好完全反应,测得物质总质量的变化如图所示,求: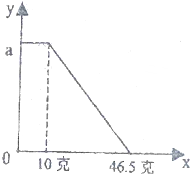 某固体物质由NaOH和MgCl2组成,取一定质量的该混合物溶于水,在所得的悬浊液中逐滴加入溶质质量分数为10%的稀盐酸,发现沉淀的质量(y)与加入盐酸的质量(x)有如图所示的关系,根据此图完成下列问题
某固体物质由NaOH和MgCl2组成,取一定质量的该混合物溶于水,在所得的悬浊液中逐滴加入溶质质量分数为10%的稀盐酸,发现沉淀的质量(y)与加入盐酸的质量(x)有如图所示的关系,根据此图完成下列问题