题目内容
8.氧化亚铜(Cu2O)可用于船底防污漆,防止海生物对船舶设备的污损,现将Cu2O和Cu的固体混合物6.8g放入烧杯中,加入过量的质量分数为20%的稀硫酸30g,充分反应后,过滤、洗涤、干燥,得到4.8g固体.已知:Cu2O+H2SO4═CuSO4+Cu+H2O.试计算:
(1)所加稀硫酸中溶质的质量为6g
(2)求通过化学反应生成的Cu的质量是1.6g(写出计算过程)
分析 (1)溶质的质量=溶液的质量乘以溶质的质量分数;
(2)由于硫酸是过量的,所以计算不可以直接使用硫酸溶质的质量,而固体反应前为6.8g,反应后变成4.8g,固体质量减少,根据方程式分析质量差进而计算.
解答 解:
(1)硫酸中溶质的质量为20%×30g=6g.
(2)设生成的铜的质量为x.
Cu2O+H2SO4═CuSO4+Cu+H2O反应前称量的固体是6.8g,为氧化亚铜和铜的混合物,反应后称量的是生成的铜和原混合物中的铜,质量为4.8g,引起质量变化是由于氧化亚铜生成铜所致.
Cu2O+H2SO4═CuSO4+Cu+H2O 固体质量变化
144 64 80
x 6.8g-4.8g=2g
$\frac{64}{80}$=$\frac{x}{2g}$ x=1.6g
答:生成的铜的质量为1.6g.
故答案为:6;1.6.
点评 分析找出计算所需要的数据,进而根据化学方程式计算.差量法计算是常用的计算方法,常用的差量法有固体质量差量,液体质量差量,还有体积差量等,平时多总结归纳.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
18. 如图表示一定质量的氯酸钾和二氧化锰固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
如图表示一定质量的氯酸钾和二氧化锰固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
 如图表示一定质量的氯酸钾和二氧化锰固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
如图表示一定质量的氯酸钾和二氧化锰固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )| A. | 氯酸钾固体的质量 | B. | 生成氧气的质量 | ||
| C. | 固体的质量 | D. | 固体中二氧化锰的质量 |
16.下列实验操作错误的是( )
| A. | 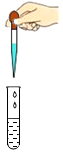 滴加液体 | B. | 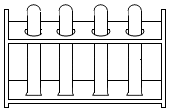 放置试管 | ||
| C. |  添加酒精 | D. | 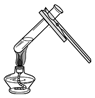 加热液体 |
13.分类是化学学习的重要方法,下列物质属于纯净物的是( )
| A. | 酸奶 | B. | 汽水 | C. | 氯酸钾 | D. | 洁净的空气 |
20.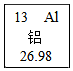 元素周期表是学习和研究化学的工具.如图是铝元素的相关信息,下列说法中不正确的是( )
元素周期表是学习和研究化学的工具.如图是铝元素的相关信息,下列说法中不正确的是( )
 元素周期表是学习和研究化学的工具.如图是铝元素的相关信息,下列说法中不正确的是( )
元素周期表是学习和研究化学的工具.如图是铝元素的相关信息,下列说法中不正确的是( )| A. | 铝是金属元素 | B. | 铝的中子数是13 | ||
| C. | 铝的质子数是13 | D. | 铝的相对原子质量是26.98 |
17.原子论和分子论学说的创立,奠定了近代化学的基础.其科学家是( )
| A. | 门捷列夫 | B. | 爱迪生 | ||
| C. | 汤姆生 | D. | 道尔顿和阿伏伽德罗 |
5.下列关于“化学”的认识不正确的是( )
| A. | 化学能够创造自然界不存在的新物质 | |
| B. | 化学能够为人类提供新能源 | |
| C. | 化学在环境保护中起重要的作用 | |
| D. | 化学的发展必然带来人类生存环境的恶化 |