题目内容
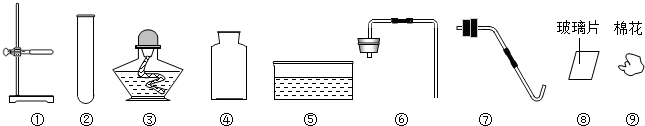
7.根据下面的装置图回答问题:
(1)写出图中标有②的仪器名称:②酒精灯.
(2)小华想用高锰酸钾制取比较纯净的氧气,他应选择的装置组合为AE(填序号).你认为A装置中还缺少棉花.加热时为什么试管口要略向下倾斜防止冷凝水倒流使试管炸裂.
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.小芳同学用加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的装置组合是AD(填序号),写出氨气和氧化铜反应的符号表达式是氧化铜+氨气$\stackrel{加热}{→}$铜+水+氮气.
分析 (1)根据常用仪器的名称即可作答;
(2)根据实验室制取氧气的反应原理、制取装置、收集装置即可作答;
(3)此题属信息题,从题干中提取信息:氨气密度比空气小,且极易溶于水,用加热氯化铵和氢氧化钙固体混合物的方法来制取.这个信息是做此题的关键;根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)根据常用仪器的名称可知答案为:②酒精灯;
(2)用高锰酸钾制取氧气需要固固加热型发生装置,故选择A装置为发生装置,CD都能用来收集氧气,但C收集的氧气不纯,所以只能用D来收集;利用高锰酸钾制取氧气时试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管;实验室用固体药品来制取氧气时,要注意连接装置时,试管口要稍微倾斜,防止防止冷凝水倒流使试管炸裂;
(3)A装置适用于固体的反应,B装置适用于固体和液体的反应,因为此题用氯化铵和氢氧化钙加热来制取氨气,所以用A装置,又因为氨气密度比空气小,且极易溶于水,所以用D装置来收集;空气中含量最多的气体是氮气,氨气和氧化铜在加热条件下反应的文字表达式为:氧化铜+氨气$\stackrel{加热}{→}$铜+水+氮气.
故答案为:(1)②酒精灯;
(2)AE,棉花,防止冷凝水倒流使试管炸裂;
(3)AD,氧化铜+氨气$\stackrel{加热}{→}$铜+水+氮气.
点评 本题综合考查实验室制取气体的原理和装置,同时考查催化剂的概念,并进行类比训练.

练习册系列答案
相关题目
15.对下列化学用语解释正确的是( )
| A. | Mg+--镁离子 | B. | O2--两个氧原子 | C. | 2H2--两个氢分子 | D. | 2N--两个氮元素 |
16.现有下列物质:①氢气;②明矾;③二氧化碳;④二氧化硫.按要求填空(只填序号):
①最清洁的燃料是①; ②能使澄清石灰水变浑浊的无色无味气体是③;
③常见的一种大气污染物是④;④常用于净水的物质是②.
①最清洁的燃料是①; ②能使澄清石灰水变浑浊的无色无味气体是③;
③常见的一种大气污染物是④;④常用于净水的物质是②.
15.复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验.
探究1:研究常见物质组成

A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素组成来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
探究3:研究常见物质制取--制取氢氧化钠溶液
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
小妮认为小欢的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是碳酸钠溶液也能使酚酞试液变红色.
小妮设计了另一个实验:
我认为:小欢和小妮的实验是为了证实小京结论的可靠性,小京的结论不可靠,原因
是氢氧化钠溶液中含有碳酸钠.显然小妮的实验可靠性比小欢的实验好,原因是排除了碳酸钠溶液的干扰.
探究1:研究常见物质组成

A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素组成来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 碳酸钠溶液 | 产生气泡 | 证明研究结论正确 |
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
小妮设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
用试管取无色溶液少许,加入过量的氯化钙溶液,再滴加适量的酚酞试液 | 酚酞试液变红色 | 无色溶液中确实 含有氢氧化钠 |
是氢氧化钠溶液中含有碳酸钠.显然小妮的实验可靠性比小欢的实验好,原因是排除了碳酸钠溶液的干扰.
2.下列变化中属于化学变化的是( )
| A. | 海水晒盐 | B. | 布料染色 | C. | 动植物的呼吸 | D. | 陶瓷破碎 |
16. 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)
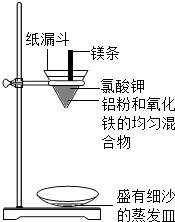
实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应.
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | Mg和CuO能反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
17. 酶是一类在常温下就可以发挥作用的生物催化剂,它的催化效能比一般化学催化剂高出几千、几万倍甚至几十万倍.土豆中含有的过氧化氢酶对过氧化氢分解具有催化作用.楚楚同学设计实验证明新鲜的土豆片也能加快过氧化氢的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,图Ⅰ为过氧化氢分解的反应装置,图Ⅱ用于测量产生O2的体积.实验时均以生成25mL气体为准,其他可能影响实验的因素均忽略不计,相关数据见下表:
酶是一类在常温下就可以发挥作用的生物催化剂,它的催化效能比一般化学催化剂高出几千、几万倍甚至几十万倍.土豆中含有的过氧化氢酶对过氧化氢分解具有催化作用.楚楚同学设计实验证明新鲜的土豆片也能加快过氧化氢的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,图Ⅰ为过氧化氢分解的反应装置,图Ⅱ用于测量产生O2的体积.实验时均以生成25mL气体为准,其他可能影响实验的因素均忽略不计,相关数据见下表:
回答下列问题:
(1)检查图Ⅱ装置气密性的方法是:关闭弹簧夹,向量气管中加水,若右侧液面高于左侧,且液面差不变,则气密性良好;
图Ⅱ装置中油层的作用是形成油封,气体将Ⅱ中液体压入量气管,从而测得产生氧气的体积(或者防止氧气溶于水,使结果不准确).
(2)上述实验中的“待测数据”指反应时间;欲探究鲜土豆片与二氧化锰的催化效果,应比较b和c (选填“a”、“b”或“c”)的大小.
 酶是一类在常温下就可以发挥作用的生物催化剂,它的催化效能比一般化学催化剂高出几千、几万倍甚至几十万倍.土豆中含有的过氧化氢酶对过氧化氢分解具有催化作用.楚楚同学设计实验证明新鲜的土豆片也能加快过氧化氢的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,图Ⅰ为过氧化氢分解的反应装置,图Ⅱ用于测量产生O2的体积.实验时均以生成25mL气体为准,其他可能影响实验的因素均忽略不计,相关数据见下表:
酶是一类在常温下就可以发挥作用的生物催化剂,它的催化效能比一般化学催化剂高出几千、几万倍甚至几十万倍.土豆中含有的过氧化氢酶对过氧化氢分解具有催化作用.楚楚同学设计实验证明新鲜的土豆片也能加快过氧化氢的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,图Ⅰ为过氧化氢分解的反应装置,图Ⅱ用于测量产生O2的体积.实验时均以生成25mL气体为准,其他可能影响实验的因素均忽略不计,相关数据见下表:回答下列问题:
| 序号 | 3%过氧化氢溶液体积 | 其他物质质量 | 待测数据 |
| ① | 20mL | 无其他物质 | a |
| ② | 20mL | 鲜土豆片0.5g | b |
| ③ | 20mL | 二氧化锰0.5g | c |
图Ⅱ装置中油层的作用是形成油封,气体将Ⅱ中液体压入量气管,从而测得产生氧气的体积(或者防止氧气溶于水,使结果不准确).
(2)上述实验中的“待测数据”指反应时间;欲探究鲜土豆片与二氧化锰的催化效果,应比较b和c (选填“a”、“b”或“c”)的大小.