题目内容
19.形象的微观示意图有助于我们认识化学物质和理解化学反应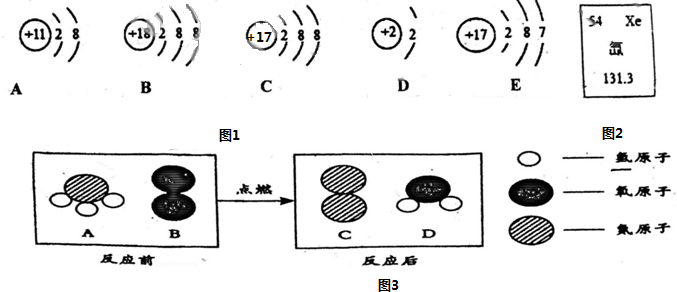
(一)如图1中A、B、C、D、E是五种粒子的结构示意图.请回答下列问題:
(1)图中属于同种元素是C、E;
(2)A、B、C、D、E五种粒子中,与B具有相似化学性质的原子是D (填序号);
(3)从E粒子结构示意图可以判断,该元素位于元素周期表的第三周期,该原子在化学反应中容易得(填“得w或“失”)电子.
(二)图2是元素周期表中氙元素的某些信息,据此可知;氙的质子数是54.相对原子质量是131.3.
(三)在宏观、微观和符号之间建立联系是化学学科的特点.
在点燃条件下,A和B反应生成C和D,反应前后分子种类变化的微观示意图如图3所示.
请回答以下问题:
①该反应属于置换反应.(填反应基本类型)
②4种物质中,属于氧化物的是D (填图中字母);
③在该反应中,生成C和D的分子个数比为1:3(计算结果用最简整数比表示)
分析 (一)(1)根据同种元素质子数相同分析;
(2)根据元素的性质与原子的最外层电子数数的关系分析;
(3)根据原子的结构与最外层电子数目的特点分析;
(二)根据元素周期表中一个格的含义分析判断;
(三)根据变化的微观示意图,分析反应物、生成物写出反应的化学方程式,据其意义分析判断有关的问题.
解答 解:(一)(1)由粒子的结构示意图可知,D、E的质子数相同,属于同种元素;
(2)B粒子的电子数等于质子数,最外层电子数目是8,达到了稳定结构,D粒子的电子数等于质子数,第一层也是最外层有2个电子,达到了稳定结构,是具有相似化学性质的原子;
(3)由E粒子结构示意图可知,该原子的核外有三个电子层,该元素位于元素周期表的第三周期,该原子的最外层电子数是7,大于4,在化学反应中容易得电子.
(二)图2是元素周期表中氙元素的某些信息,据此可知;氙的质子数是54.相对原子质量是131.3.
(三)由变化的微观示意图可知,该反应是氨气燃烧生成了氮气和水,反应的化学方程式是:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
①该反应由一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;
②4种物质中D是水,是由氢和氧两种元素组成的,属于氧化物;
③由方程式可知,在该反应中,生成C和D的分子个数比为:2:6=1:3
故答为:(一)(1)DE;(2)D;(3)三,得.(二)54,131.3.(三)①置换;②D;③1:3
点评 解答本题要掌握化学方程式的书写方法和图中提供的信息,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 纯水是中性的,所以它的pH等于7 | |
| B. | 银跟盐酸起反应,生成氯化银和氢气 | |
| C. | 混有水蒸气的CO2通过NaOH固体后,得到干燥的CO2 | |
| D. | 凡能电离产生OH-离子的化合物叫做碱 |
14.下到事实和相应的解释一致的是( )
| A. | 真金不怕火炼一一说明金的熔点很高: | |
| B. | 干冰升华变为气体,所占体积变大--气体分子变大 | |
| C. | 金刚石用于钻探矿层--金刚石硬度大: | |
| D. | 燃烧的蜡烛被吹灭--可燃物与空气隔绝 |
11.下列实验操作正确的是( )
| A. | 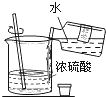 稀释浓硫酸 | B. | 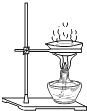 蒸发食盐水 | ||
| C. |  套橡胶管 | D. | 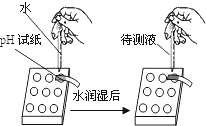 测溶液pH |
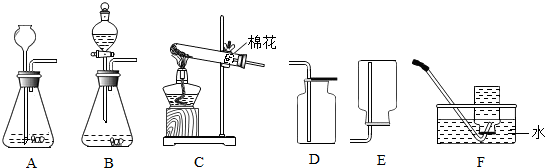
8.常温下NO易与空气中氧气反应,难溶于水,密度大于空气,收集NO气体用( )
| A. | 向上排空气法 | B. | 向下排空气法 | ||
| C. | 排水法 | D. | 排水法或向上排空气法 |
9.过氧化钠(Na2O2)可用作呼吸面积的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】③取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是NaOH、Na2CO3(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在.
【定量研究】
称取6.04g过氧化钠药品于锥形瓶中,加入适量蒸馏水使固体完全溶解,共收集到0.64g气体;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g.
(1)写出加入澄清石灰水发生反应的化学方程式:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(2)6.04g上述样品中含有NaOH的质量为0.8g.
【反思提高】
过氧化钠长时间露置在空气中会全部变质,最终转化为Na2CO3(填化学式).
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
【实验探究】③取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是NaOH、Na2CO3(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在.
【定量研究】
称取6.04g过氧化钠药品于锥形瓶中,加入适量蒸馏水使固体完全溶解,共收集到0.64g气体;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g.
(1)写出加入澄清石灰水发生反应的化学方程式:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(2)6.04g上述样品中含有NaOH的质量为0.8g.
【反思提高】
过氧化钠长时间露置在空气中会全部变质,最终转化为Na2CO3(填化学式).
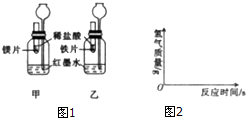 控制变量法是常用的化学学习方法,下面是某小组探究活动的过程:已知试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.在室温条件下进行如图1所示实验.
控制变量法是常用的化学学习方法,下面是某小组探究活动的过程:已知试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.在室温条件下进行如图1所示实验.