题目内容
2.现有二瓶气体,一瓶是一氧化碳,一瓶是二氧化碳.当瓶中的CO和瓶中的CO2分子数相同时,则瓶中的CO和瓶中的CO2中氧元素的质量比为1:2,当瓶中的CO和瓶中的CO2质量相同时,则瓶中的CO和瓶中的CO2中氧元素的质量比为11:14,当瓶中的CO和瓶中的CO2中含有相同质量的氧元素时,则瓶中的CO和瓶中的CO2的质量比是14:11.分析 根据同种元素的原子个数比即为元素的质量比结合物质的相对分子质量来分析解答.
解答 解:瓶中的CO和瓶中的CO2分子数相同,均可认为是1个分子时,则一个一氧化碳分子中含有1个氧原子,一个二氧化碳分子中含有2个氧原子,则瓶中的CO和瓶中的CO2中氧元素的质量比为1:2;故填:1:2;
若瓶中的CO和瓶中的CO2质量相同,可设CO和CO2的质量为m,则等质量的CO和CO2中所含氧元素的质量比是(m×$\frac{16}{28}$×100%):(m×$\frac{16×2}{44}$×100%)=11:14;故填:11:14;
因为2分子CO里面所含的氧原子个数与1分子CO2里面的一样都为2个;所以一份CO2里面的氧元素的质量和两份CO里面氧元素的质量是一样的;因此两份CO的质量与一份CO2的质量比为:(12+16)×2:(12+16+16)=56:44=14:11;故填:14:11.
点评 本题主要考查考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
12.下列各组物质的溶液混合后能发生复分解反应,但不产生沉淀和气体的是( )
| A. | 氢氧化钙和盐酸 | B. | 硝酸钾和硫酸钠 | ||
| C. | 碳酸钙和盐酸 | D. | 氯化铁和氢氧化钠 |
17.氮元素有多种可变化合价.在NH4NO3、N2、NO2、NO、NaNO2这五种物质中N元素表现出的化合价共有( )
| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
14.某校科学兴趣小组的同学对五个品牌味精(A、B、C、D、E)中NaCl的含量进行测定.下面是该小组所做的实验步骤:
①称取某种品牌味精样品m克放入烧杯中,加适量蒸馏水完全溶解.
②加入足量稀硝酸和硝酸银溶液(待填).
③过滤,用蒸馏水洗涤沉淀2-3次.
④将沉淀烘干、称量,测得固体质量为m1克.
⑤实验数据记录.
(1)补齐实验步骤②加入足量稀硝酸和硝酸银溶液
(2)求D品牌味精中NaCl的质量分数.
| 味精品牌 | A | B | C | D | E |
| 样品质量m(克) | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 |
| 沉淀质量m1(克) | 4.7 | 4.8 | 4.8 | 4.9 | 5.2 |
②加入足量稀硝酸和硝酸银溶液(待填).
③过滤,用蒸馏水洗涤沉淀2-3次.
④将沉淀烘干、称量,测得固体质量为m1克.
⑤实验数据记录.
(1)补齐实验步骤②加入足量稀硝酸和硝酸银溶液
(2)求D品牌味精中NaCl的质量分数.
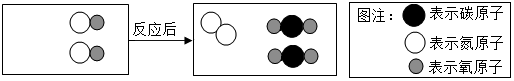

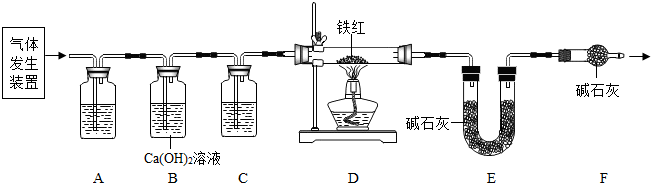
 小李用图1气体发生装置来制取二氧化碳,老师给他提供了石灰石、稀盐酸.小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图2所示,最后还有少量石灰石剩余.(不计水蒸发和稀盐酸的挥发且2HCl+CaCO3═CaCl2+H2O+CO2↑)
小李用图1气体发生装置来制取二氧化碳,老师给他提供了石灰石、稀盐酸.小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图2所示,最后还有少量石灰石剩余.(不计水蒸发和稀盐酸的挥发且2HCl+CaCO3═CaCl2+H2O+CO2↑)