题目内容
3.实验室常用下列装置来制取氧气: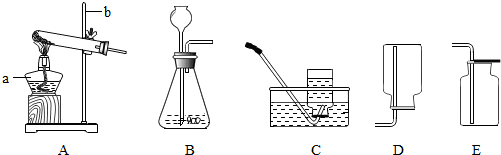
(1)写出图中有标号仪器的名称:a试管、b铁架台.
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)质量分数为3%的医用双氧水在常温下难分解;但在双氧水溶液中加入铁锈,就会迅速分解,且反应结束后过滤出的铁锈可重复使用.试写出该反应的化学方程式2H2O2$\frac{\underline{\;铁锈\;}}{\;}$2H2O+O2↑;用该发生装置还可以制取的气体是二氧化碳、氢气(从学过的气体中选择).
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.
①制取氨气反应的方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2X.X的化学式为:H2O.
②制取并收集NH3,应该从如图中选择的发生装置是A,收集装置是D.
③NH3是一种碱性气体,干燥时不能选用下列干燥剂中的B(填序号).
A.固体氢氧化钠 B.浓硫酸 C.生石灰.
分析 (1)根据实验室常仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用过氧化氢和二氧化锰制取氧气的反应物是固体和液体,反应条件是常温,二氧化锰是该反应的催化剂进行分析;
(3)根据过氧化氢在铁锈的催化作用下生成水和氧气,结合学过的固体和液体反应常温型的气体进行分析;
(5)①根据质量守恒定律进行分析;
②根据实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,极易溶于水进行分析;
③根据氨气是碱性气体,不能用酸性干燥剂干燥进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是试管,b是铁架台;
(2)实验室用过氧化氢和二氧化锰制取氧气的反应物是固体和液体,反应条件是常温,所以选用的发生装置是B,二氧化锰是该反应的催化剂,起催化作用;
(3)过氧化氢在铁锈的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;铁锈\;}}{\;}$2H2O+O2↑,用该发生装置还可以制取的气体是:二氧化碳、氢气;
(5)①在化学反应前后原子个数不变,反应物中有2个氮原子,10个氢原子,2个氯原子,1个钙原子,1个氧原子,生成物中有1个钙原子,2个氯原子,2个氮原子,6个氢原子,所以X是H2O;
②实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,极易溶于水,所以发生装置是A,收集装置是D;
③氨气是碱性气体,不能用酸性干燥剂干燥,故选:B.
故答案为:(1)酒精灯,铁架台;
(2)B,催化;
(3)2H2O2$\frac{\underline{\;铁锈\;}}{\;}$2H2O+O2↑,二氧化碳、氢气;
(5)①H2O;
②A,D;
③B.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | 铁元素的原子核内的质子数为26 | B. | 铁元素的原子核内的中子数为26 | ||
| C. | 铁元素的原子核外电子数为30 | D. | 铁元素的原子的质量为56 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 除去硝酸镁中的硝酸银,加入过量的铁粉 | |
| B. | 提纯新制二氧化碳中的氯化氢气体,将气体通过氢氧化钠溶液 | |
| C. | 鉴别生石灰中是否含有未分解的石灰石,加入稀盐酸 | |
| D. | 鉴别食盐水和醋酸,加入无色酚酞,观察颜色 |
| A. | 金刚石 | B. | 石墨 | C. | C60 | D. | 炭黑 |
| A. |  滴加液体 | B. |  滴定用完清洗放回原瓶 | ||
| C. | 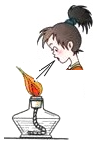 熄灭酒精灯 | D. |  将固体粉末放入试管 |