题目内容
11.下列实验方法可行的是( )| A. | 除去硝酸镁中的硝酸银,加入过量的铁粉 | |
| B. | 提纯新制二氧化碳中的氯化氢气体,将气体通过氢氧化钠溶液 | |
| C. | 鉴别生石灰中是否含有未分解的石灰石,加入稀盐酸 | |
| D. | 鉴别食盐水和醋酸,加入无色酚酞,观察颜色 |
分析 A、根据铁和硝酸银反应生成硝酸亚铁和银进行分析;
B、根据二氧化碳、氯化氢都会与氢氧化钠溶液反应进行分析;
C、根据碳酸钙会与稀盐酸反应生成二氧化碳进行分析;
D、根据酚酞在酸性、中性液体中都不会变色进行分析.
解答 解:A、铁和硝酸银反应生成硝酸亚铁和银,除去了杂质硝酸银,又引入新的杂质硝酸亚铁,故A错误;
B、二氧化碳、氯化氢都会与氢氧化钠溶液反应,杂质和主要物质都会被除去,故B错误;
C、取样品,加入稀盐酸,有气泡产生,证明有碳酸钙,反之,没有碳酸钙,可以鉴别,故C正确;
D、酚酞在酸性、中性液体中都不会变色,所以酚酞不能鉴别食盐水和醋酸,故D错误.
故选:C.
点评 本题难度不大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下面各连线是对某一主题知识进行归纳的情况,其中有错误的是( )
| A. | 溶洞探险--须做灯火实验 | B. | 活性炭有吸附性--做净水剂 | ||
| C. | 减少酸雨发生--使用新型能源 | D. | 检查煤气泄露--用燃着火把 |
18.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究.
(1)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】A.溶质可能是CaCl2与Ca(OH)2B.溶质可能只是CaCl2
C.溶质可能是CaCl2与盐酸
【实验探究】
①小明同学从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他排除了猜想A,你认为他排除猜想A的理由是氢氧化钙溶液呈碱性.
②小华同学想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,并填写以下表格:
通过以上探究,最后确定猜想C正确.
【反思与拓展】
你认为上述烧杯内溶液如果未经处理直接倒入铁制下水道,可能造成的危害是腐蚀下水道.要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的碳酸钙,充分反应后过滤.化学反应方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
有一种未知浓度的稀硫酸100g,向其中假如足量的锌粉,充分反应后过滤,反应中共收集到氢气0.2g.试计算该硫酸溶液的质量分数是多少?
(1)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】A.溶质可能是CaCl2与Ca(OH)2B.溶质可能只是CaCl2
C.溶质可能是CaCl2与盐酸
【实验探究】
①小明同学从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是他排除了猜想A,你认为他排除猜想A的理由是氢氧化钙溶液呈碱性.
②小华同学想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,并填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液 | 立即产生白色沉淀 开始有气泡产生,然后有白色沉淀生成 | 猜想B正确 猜想C正确 |
【反思与拓展】
你认为上述烧杯内溶液如果未经处理直接倒入铁制下水道,可能造成的危害是腐蚀下水道.要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的碳酸钙,充分反应后过滤.化学反应方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
有一种未知浓度的稀硫酸100g,向其中假如足量的锌粉,充分反应后过滤,反应中共收集到氢气0.2g.试计算该硫酸溶液的质量分数是多少?
6.下列实验方案的设计中,没有正确体现对比这种科学思想的是( )
| A. | 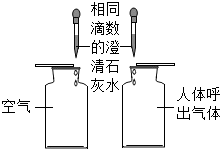 比较二氧化碳的含量 | B. | 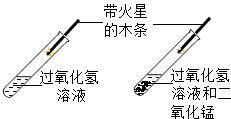 研究二氧化锰的催化作用 | ||
| C. | 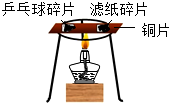 比较不同物质的着火点 | D. | 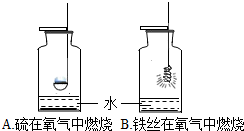 实验中水的作用 |
20.下列物质是按照单质、氧化物、混合物的顺序排列的是( )
| A. | 氨气、干冰、洁净的空气 | B. | 氢气、冰水、洁净的海水 | ||
| C. | 水银、氨水、高锰酸钾 | D. | 液氧、蒸馏水、稀有气体 |
1.下列变化中属于化学变化的是( )
| A. | 水结成冰 | B. | 铁生锈 | C. | 酒精挥发破 | D. | 瓷碗碎 |