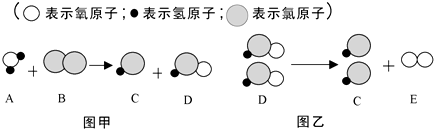
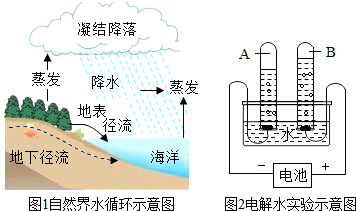
题目内容
为测定锌铜合金中锌的含量,取该合金放入盛有稀硫酸的锥形瓶中,充分反应.多次实验后,取平均值所得数据如下表:
计算:
(1)求生成氢气的质量?
(2)该合金中锌的质量分数?
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
(1)求生成氢气的质量?
(2)该合金中锌的质量分数?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据锌和硫酸反应生成氢气而铜不反应,所以反应前后质量减少的质量就是氢气的质量进行解答;
(2)根据氢气的质量求出该合金中锌的质量以及该合金中锌的质量分数进行解答.
(2)根据氢气的质量求出该合金中锌的质量以及该合金中锌的质量分数进行解答.
解答:解:(1)依题意可得
氢气的质量=342.10g+16.00g-357.70g
=0.4g
答:氢气的质量为0.4g
(2)设该合金中锌的质量分数为x.
Zn+H2SO4 ═ZnSO4+H2↑
65 2
16.00g×x 0.4g
=
x=81.25%
答:该合金中锌的质量分数为81.25%.
氢气的质量=342.10g+16.00g-357.70g
=0.4g
答:氢气的质量为0.4g
(2)设该合金中锌的质量分数为x.
Zn+H2SO4 ═ZnSO4+H2↑
65 2
16.00g×x 0.4g
| 65 |
| 2 |
| 16g×x |
| 0.4g |
x=81.25%
答:该合金中锌的质量分数为81.25%.
点评:解此题的关键是审清题意,找出突破口,再结合方程式进行计算,可以得到问题答案.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
已知R2-核外电子数为X个,其相对原子质量为M,则R2-中含有的中子数为( )
| A、M-X-2 | B、M-2 |
| C、X-2 | D、M-X+2 |
鉴别空气、氧气、二氧化碳三瓶气体,最简单的方法( )
| A、将带火星的木条分别伸入集气瓶 |
| B、将气体分别通入澄清石灰水中 |
| C、将气体分别通入水中 |
| D、将燃着的木条分别伸入集气瓶 |
正确量取12mL液体,应选用的一组仪器是( )
①15mL量筒 ②10mL量筒 ③20mL量筒 ④胶头滴管.
①15mL量筒 ②10mL量筒 ③20mL量筒 ④胶头滴管.
| A、③④ | B、①④ | C、②④ | D、①②④ |
现有10g某金属样品(杂质不与酸反应,也不溶于水),与l00克质量分数9.8%的稀硫酸恰好完全反应,过滤,将得到的溶液蒸干,得到16.1g固体.则该样品中金属的质量分数为( )
| A、90% | B、80% |
| C、65% | D、50% |
下列有关“一定”和“不一定”说法中不正确的是( )
| A、原子核内一定含有中子 |
| B、同种元素的原子和离子质子数一定相同 |
| C、氧化反应不一定是化合反应 |
| D、生成两种物质的反应不一定是分解反应 |
根据下面四种粒子的结构示意图判断以下说法正确的是( )
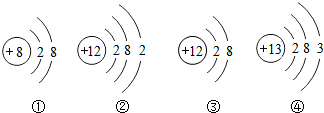

| A、①图是一种稀有气体元素的原子结构示意图 |
| B、②图所示的粒子是一种离子 |
| C、②③两图所示的粒子化学性质相似 |
| D、③④两图表示的是两种不同元素的粒子 |