题目内容
现有10g某金属样品(杂质不与酸反应,也不溶于水),与l00克质量分数9.8%的稀硫酸恰好完全反应,过滤,将得到的溶液蒸干,得到16.1g固体.则该样品中金属的质量分数为( )
| A、90% | B、80% |
| C、65% | D、50% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据质量守恒定律,生成的硫酸盐中的硫酸根的质量与恰好完全反应的稀硫酸中硫酸根质量相等,而硫酸盐中的金属质量也与金属样品中金属质量相等.
解答:解:100g质量分数为19.6%的稀硫酸中硫酸根的质量=100g×9.8%×
×100%=9.6g;
16.1g硫酸盐中金属元素的质量=16.1g-9.6g=6.5g;
则样品中含金属的质量分数=
×100%=65%.
故选:C.
| 96 |
| 98 |
16.1g硫酸盐中金属元素的质量=16.1g-9.6g=6.5g;
则样品中含金属的质量分数=
| 6.5g |
| 10g |
故选:C.
点评:本题解题技巧就在于:根据质量守恒定律,分析出硫酸盐中金属元素质量与金属样品中金属质量相等,硫酸盐中硫酸根质量与硫酸中硫酸根质量相等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.下列说法正确的是( )
| A、二氧化钛中Ti的化合价为+2 |
| B、萘胺中C、H、N的原子个数比为10:9:1 |
| C、二氧化钛中钛元素的质量分数为30% |
| D、这种试纸是一种新型化合物 |
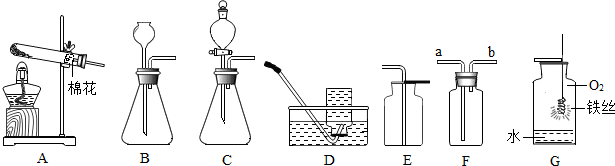
规范的实验操作是实验成功的基础,以下操作正确的是( )
A、 液体的倾倒 |
B、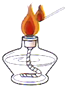 点燃酒精灯 |
C、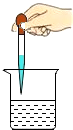 滴加液体 |
D、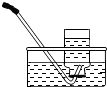 排水集气 |
下列叙述正确的是( )
| A、因为“质量守恒”,所以煤燃烧后产生的煤渣的质量一定和所用煤的质量相等 |
| B、铁丝在氧气中燃烧后,生成物的质量比铁丝的质量增加了 |
| C、100克酒精和100克水混合在一起后,质量等于200克,符合质量守恒定律 |
| D、H2和O2形成混合物的质量等于其反应后生成水的质量 |
下列叙述正确的是( )
| A、一种元素组成的物质可能是混合物也可能是单质,一定不是化合物 |
| B、分子可以再分,原子不可以再分 |
| C、用刀切西瓜的过程中,部分分子被分成了原子 |
| D、带电的微粒都称为离子 |
将河水转变为供饮用的自来水的主要程序有:①化学沉降(用明矾);②消毒杀菌(用漂白粉);③自然沉降;④加热煮沸.合理的顺序是( )
| A、③②①④ | B、③①②④ |
| C、③①④② | D、①③④② |