题目内容
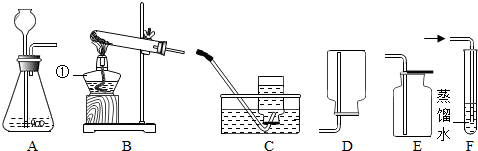
12.下列实验方案能达到目的是( )| A. |  探究燃烧的三个条件 | B. |  探究铁生锈的条件 | ||
| C. |  探究二氧化锰对反应速率的影响 | D. |  测定空气里氧气含量 |
分析 A、根据燃烧的条件来考虑实验是否能达到目的;
B、根据铁生锈的条件来考虑;
C、根据对照试验的设计方法考虑;
D、根据铜和氧气反应生成氧化铜固体考虑.
解答 解:A、不能验证燃烧的条件中可燃物与氧气接触,在水下放上白磷,故A错误;
B、铁生锈的条件是与氧气和水共同接触,该实验缺少将干燥的铁钉放到干燥的试管内,用橡皮塞塞上试管口,验证没有水是否能生锈,故B错误;
C、对照试验,一个放二氧化锰,一个不放二氧化锰,但是放二氧化锰的过氧化氢溶液浓度高,反应快还有可能是与过氧化氢溶液的有关,所以不能达到实验目的,故C错误;
D、铜和氧气反应生成氧化铜固体,所以可用足量的铜测定空气里氧气含量,故D正确.
故选D.
点评 解答本题关键是要知道燃烧条件的实验设计方法,铁生锈条件验证实验设计,了解对照试验的设计思路.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
3. 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 甲的溶解度受温度影响比乙大 | |
| B. | 20℃时,甲溶液的溶质质量分数比乙大 | |
| C. | 20℃时,将25g甲加入50g水中,可形成75g溶液 | |
| D. | 将30℃时甲的饱和溶液降温至20℃,会有20g晶体析出 |
17.大多数花卉喜欢微酸性土壤,某花卉长势不佳,经测定盆中土壤pH为8.2,在施用较稀FeSO4溶液浇灌后长势良好,这说明FeSO4溶液( )
| A. | 显碱性 | B. | 显酸性 | C. | 显中性 | D. | 无法判断 |