题目内容
15.某化学课外小组的同学,在实验室发现四瓶标签破损的无色溶液(如图所示),其中A、B试剂瓶标签部分破损,C、D试剂标签完全破损,根据查阅药品记录表可知,A、B、C、D分别是NaOH溶液、Na2CO3溶液、石灰水、CaCl2溶液中的一种.在老师的指导下,化学课外小组同学进行了下述实验.老师给准备的试剂有:稀盐酸、NaHCO3溶液和酚酞溶液.

(1)分别取A、B、C、D溶液于4支试管中,向其中分别滴加酚酞溶液,发现A、B、C溶液变红,说明这3种溶液呈碱性(填“酸性”、“碱性”或“中性”),由该实验可确定的溶液为D CaCl2溶液(填试剂瓶序号及相应的溶液名称).
(2)分别取A、B溶液于两支试管中,加入足量的稀盐酸,发现均有气泡产生,小组同学利用上述共计7种试剂,经过下述实验最终确定了两种溶液的成分.
| 实验操作 | 现象 | 实验结论 |
| ①分别取A、B溶液于2支试管中,向其中分别滴加CaCl2溶液; ②过滤后,分别向滤液中滴加酚酞溶液 | 白色沉淀 A:滤液无明显变化 B:滤液变成红色 | A是Na2CO3溶液 B是变质的NaOH溶液 |
(3)取C溶液于试管中,逐渐滴加一定量的NaHCO3溶液,充分反应,观察到溶液变浑浊,过滤、滤液中除了OH-外,还含有较大量的阳离子是Na+、Ca2+(填离子符号).
查阅资料可知:Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O
NaOH+NaHCO3=Na2CO3+H2O.
分析 (1)根据显碱性的溶液能使酚酞试液变红色;氢氧化钠溶液、碳酸钠溶液、石灰水等物质显碱性,氯化钙溶液显中性解答;
(2)根据实验结论可以判断出现的实验现象;氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
(3)根据石灰水中的氢氧化钙和碳酸氢钠溶液中的碳酸氢钠的质量情况可以判断滤液中溶质的组成情况.
解答 解:
(1)A、B、C溶液变红,说明这3种溶液呈碱性,由该实验可确定D是CaCl2溶液.
(2)实验操作及现象:分别取适量A、B溶液于两支试管中,加入过量CaCl2溶液,均产生白色沉淀,过滤,分别向滤液中滴入酚酞溶液溶液,A滤液无明显变化,B滤液变成红色;实验结论:A溶液是Na2CO3溶液,B溶液是变质的NaOH溶液;
碳酸钠和稀盐酸反应的化学方程式分别为:NaOH+HCl═NaCl+H2O;
(3)C是石灰水,石灰水中的氢氧化钙和碳酸氢钠反应,当氢氧化钙过量时,溶液变浑浊,反应的方程式为:Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O,此时滤液中溶质是氢氧化钠和氢氧化钙;过滤、滤液中除了OH-外,还含有较大量的阳离子是Na+、Ca2+;
答案:
(1)碱性 D CaCl2溶液
(2)
| 实验操作 | 现象 | 实验结论 |
| ①分别取A、B溶液于2支试管中,向其中分别滴加 CaCl2溶液; ②过滤后,分别向滤液中滴加 酚酞溶液 | 白色沉淀 A:滤液无明显变化 B:滤液变成红色 | A是Na2CO3溶液 B是变质的NaOH溶液 |
(3)Na+、Ca2+
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
3.下列做法科学的是( )
| A. | 用盐酸可以去除生石灰中的少量CaCO3 | |
| B. | 用燃烧法可以区别涤纶和羊毛 | |
| C. | 用稀硫酸可以除去铁粉中混有的少量氧化铜 | |
| D. | 用Ba(NO3)2溶液可以除去稀盐酸中少量的H2SO4 |
20.化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的.下列实验操作或设计中正确的是( )
| A. |  用100mL量筒量取8.5mL盐酸 用100mL量筒量取8.5mL盐酸 | B. |  收集氢气 收集氢气 | ||
| C. |  验证质量守恒定律 验证质量守恒定律 | D. |  分离碘酒中的碘 分离碘酒中的碘 |
1.四氟乙烯(C2F4)中氟元素的化合价是-1价,则碳元素的化合价与下列哪种物质中碳元素的化合价相同( )
| A. | C | B. | CH4 | C. | CO | D. | CO2 |
2.学好化学,能使我们更清楚地认识世界.下列有关说法中不正确的是( )
| A. | 电解水实验中是把电能转化成化学能 | |
| B. | 本饮品纯天然,绝对不含任何化学物质 | |
| C. | 检查装置气密性时,先用手紧捂试管,后将导管伸入水中 | |
| D. | 实验室制取二氧化碳时,先加石灰石,后加稀盐酸 |
 如图是利用数字化传感器得到的盐酸和氢氧化钙反应过程中溶液pH变化图象.
如图是利用数字化传感器得到的盐酸和氢氧化钙反应过程中溶液pH变化图象.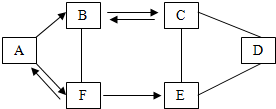 A-F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质,(部分反应物,生成物及反应条件已略去)请回答:
A-F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质,(部分反应物,生成物及反应条件已略去)请回答: