题目内容
8.化学实验中经常用到一定溶质质量分数的溶液.请回答:(1)某同学要在实验室配制15%的氯化钠溶液50g.需要氯化钠的质量为7.5克,该同学按下图所示步骤依次操作:
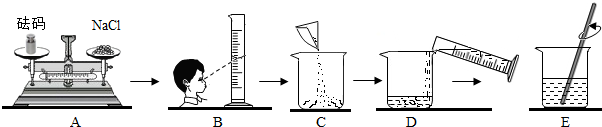
其中操作错误的步骤是AB(填字母);E中玻璃棒的作用是搅拌,加速溶解.
(2)若如图A中砝码的质量为5g,游码为2.5g,则该同学称得的氯化钠质量实际为2.5克.
分析 (1)根据溶质质量分数公式可以计算出所需氯化钠的质量,以及用托盘天平时应左物右码,量筒读数时应使视线与凹液面的最低处保持水平解答;
(2)根据根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,列等式进行计算.
解答 解:(1)需氯化钠的质量为50g×15%=7.5g;
使用托盘天平时应左物右码,量筒读数时应使视线与凹液面的最低处保持水平,在此实验中玻璃棒的作用为搅拌,其目的为加速溶解;
(2)托盘天平中左盘的质量=右盘的质量+游码的质量,因为称量时药品与砝码放反了,所以药品的实际质量为5g-2.5g=2.5g.
故答案为:(1)7.5,AB,搅拌,加速溶解;
(2)2.5.
点评 本题考查的是溶液的配制,完成此题,可以依据已有的知识进行回答,所以要求同学们在平时的学习中要加强基础知识的储备.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.根据下列实验装置图,回答问题.
(1)写出图中仪器a的名称:铁架台.
(2)实验室用氯酸钾和二氧化锰混合物制取氧气的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,应选择的发生装置为A(填字母).
(3)实验室常用大理石或石灰石和稀盐酸反应制取二氧化碳气体,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的②口(填“①”或“②”)通入.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室用氯酸钾和二氧化锰混合物制取氧气的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,应选择的发生装置为A(填字母).
(3)实验室常用大理石或石灰石和稀盐酸反应制取二氧化碳气体,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的②口(填“①”或“②”)通入.
3.人类利用金属矿物历史久远.
(1)现代冶炼技术用CO与赤铁矿石反应来冶炼生铁,请写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
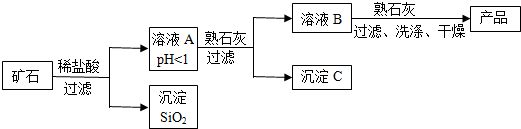
①溶液A中共含有4种阳离子;
②在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为是6.7≤pH<8.6;
③溶液B中一定含有的溶质为MgCl2、CaCl2(填化学式).
(1)现代冶炼技术用CO与赤铁矿石反应来冶炼生铁,请写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:

①溶液A中共含有4种阳离子;
②在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为是6.7≤pH<8.6;
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
20.安徽是农业大省,水稻是安徽省的主要粮食作物之一.下列有关水稻种植过程及其相关应用的叙述中涉及到化学变化的是( )
| A. |  栽种秧苗 | B. |  收割水稻 | C. |  稻谷晾晒 | D. |  稻草发电 |
17.铝合金、氧化铝、硫酸铝三种物质的分类正确的是( )
| A. | 混合物、氧化物、盐 | B. | 混合物、盐、化合物 | ||
| C. | 单质、混合物、盐 | D. | 金属单质、氧化物、纯净物 |

 A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:
A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题: