题目内容
7.加热一定质量的高锰酸钾,测得反应过程中固体质量变化如表所示:| 反应时间 | 0 | tl | t2 | t3 | t4 |
| 固体质量/g | 15.8 | 15.2 | 14.7 | 14.2 | 14.2 |
(2)反应前后,固体中氧元素的质量减小g(选填“增加”、“减小”或“不变”).
(3)通过计算确定最后所得14.2g固体的组成(写出计算过程).
分析 根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,依据固体减少的质量就是氧气的质量进行计算.
解答 解:(1)由质量守恒定律可知,生成氧气的质量为:15.8g-14.2g=1.6g;
(2)高锰酸钾分解生成了氧气,所以反应前后,固体中氧元素的质量减小;
(3)设参加反应的高锰酸钾的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 1.6g
$\frac{316}{x}$=$\frac{32}{1.6g}$
x=15.8g
所以反应后高锰酸钾完全分解,所得14.2g固体的组成是锰酸钾和二氧化锰.
故答案为:(1)1.6g;
(2)减小;
(3)所得14.2g固体的组成是锰酸钾和二氧化锰.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
15.如图所示装置所示的实验中,能达到实验目的是( )(已知浓硫酸具有吸水性,可作为某些气体干燥剂)
| A. | 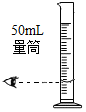 量取9.3mL稀盐酸 | |
| B. | 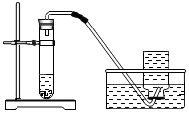 用过氧化氢溶液与二氧化锰制取少量氧气 | |
| C. | 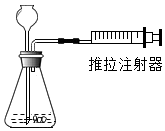 检查装置气密性 | |
| D. | 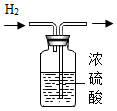 除去水中H2中的水蒸气 |
19.下列化学方程式书写正确的是( )
| A. | Mg+O2═MgO2 | B. | C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | ||
| C. | .H2O2═H2+O2 | D. | CO2+Ca(OH)2═CaC03+H2O |
16.某兴趣小组加热氯酸钾和二氧化锰混合物共15g制取氧气,试管中固体质量随时间变化数据如表:
(1)生成氧气的质量为4.8g
(2)计算生成氯化钾的质量.
(3)加热到t2时,固体混合物中钾元素的质量为3.9g.
| 加热时间/s | t1 | t2 | t3 | t4 | t5 |
| 固体质量/g | 14.0 | 11.6 | 10.8 | 10.2 | 10.2 |
(2)计算生成氯化钾的质量.
(3)加热到t2时,固体混合物中钾元素的质量为3.9g.
17.一定条件下,在密闭容器中发生某反应,测得反应过程中的部分数据如表所示.
①~④未知数据计算正确的是( )
①~④未知数据计算正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量(g) | 10 | 10 | 0 | 0 |
| 反应中的质量(g) | 6 | 2 | 3 | ① |
| 反应后的质量(g) | ② | 0 | ③ | ④ |
| A. | ①为7 | B. | ②为4 | C. | ③为3.75 | D. | ④为16.25 |