题目内容
4. 下列说法正确的是( )
下列说法正确的是( )| A. | 钠元素属于非金属元素 | B. | 钠原子核外有一个电子 | ||
| C. | 钠的相对原子质量为ll | D. | 钠原子在化学反应中易失电子 |
分析 根据元素周期表、原子结构示意图等方面的内容进行分析、判断.
解答 解:
A、可以根据钠原子最外层电子数是1,<4,属于金属元素,或者直接观察“钠”带金字旁,属于金属元素,错误;
B、该原子的最外层电子数是1个,核外有11个电子,错误;
C、最下面的数值是相对原子质量,该元素的相对原子质量是22.99,错误;
D、该原子的最外层电子数是1个,在反应中容易失去电子正确.
故选D.
点评 本题考查学生对元素周期表的理解及对原子结构示意图的认识,清楚每部分所表达的含义,即可顺利解答.

练习册系列答案
相关题目
15.某化学兴趣小组用如图装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究.
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O):氧化亚铜是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O.
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
①全部是铜;
②全部是氧化亚铜;
③是两者的混合物.
【实验探究】
(1)用图1装置完成木炭还原氧化铜的实验,观察到澄清石灰水变浑浊,写出该反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
(2)试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
【反思与评价】木炭还原氧化铜的实验中,生成的气体可能含有一氧化碳,为了防止对空气造成污染,可将图1虚线方框内的装置改为图2中的ABD(选填字母).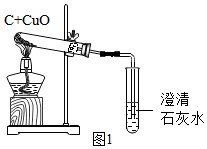
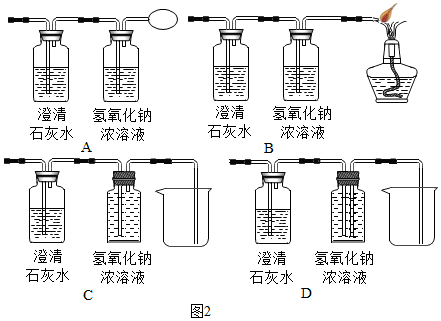
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O):氧化亚铜是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O.
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
①全部是铜;
②全部是氧化亚铜;
③是两者的混合物.
【实验探究】
(1)用图1装置完成木炭还原氧化铜的实验,观察到澄清石灰水变浑浊,写出该反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
(2)试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
| 步骤 | 现象 | 结论 |
| ①取1.8g红色固体于试管中,滴加足量稀硫酸,充分反应 | 溶液由无色变蓝色 | 猜想①错误 |
| ②过滤,将滤渣洗涤、干燥、称量 | 所得固体质量大于0.8g | 猜想③正确 |


12.下列化学方程式书写正确的是( )
| A. | 2Fe+6HCl═2 Fe Cl 3+3H2↑ | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | Cu+Ag(NO3)2═NO3)2+Ag | D. | Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$MgO2 |
9.能将蒸馏水、稀硫酸、稀氢氧化钠溶液鉴别出来的物质是( )
| A. | 铁丝 | B. | 澄清石灰水 | C. | 无色酚酞 | D. | 紫色石蕊 |
13.下列制备氯化铜的方法正确的是( )
| A. | 铜和稀盐酸反应 | B. | 铜和稀硫酸反应后,再加稀盐酸 | ||
| C. | 氢氧化铜和稀盐酸反应 | D. | 氧化铜和稀硫酸反应 |
14.要配制100g5%的NaCl溶液,除需要托盘天平和量筒外,还需要用到的一组仪器是( )
| A. | 烧杯、试管、玻璃棒 | B. | 烧杯、酒精灯、玻璃棒 | ||
| C. | 烧杯、胶头滴管、玻璃棒 | D. | 烧杯、胶头滴管、漏斗 |
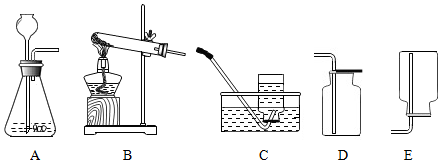
 某同学用如图的装置测定空气中氧气的体积分数.
某同学用如图的装置测定空气中氧气的体积分数.