题目内容
取24克大理石放入烧杯中,加入一定量的10%的稀盐酸,恰好完全反应,收集到二氧化碳的质量是8.8克,求
(1)大理石中碳酸钙的质量分数;
(2)所用稀盐酸溶液的质量;
(3)配制10%的这种稀盐酸需要38%的盐酸(密度为1.1g/cm3)多少毫升?
(1)大理石中碳酸钙的质量分数;
(2)所用稀盐酸溶液的质量;
(3)配制10%的这种稀盐酸需要38%的盐酸(密度为1.1g/cm3)多少毫升?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:有关化学方程式的计算
分析:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据二氧化碳的质量可以计算碳酸钙的质量、反应的氯化氢中质量,进一步可以计算大理石中碳酸钙的质量分数和所用稀盐酸溶液的质量;
溶液稀释前后,溶质质量不变.
溶液稀释前后,溶质质量不变.
解答:解:(1)设碳酸钙的质量为x,反应的氯化氢的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 8.8g
=
=
,
x=20g,y=14.6g,
大理石中碳酸钙的质量分数为:
×100%≈83.3%,
答:大理石中碳酸钙的质量分数为83.3%.
(2)所用稀盐酸溶液的质量为:14.6g÷10%=146g,
答:所用稀盐酸溶液的质量为146g.
(3)设需要38%的盐酸的体积为z,
根据题意有:z×1.1g/cm3×38%=13.6g,
z=32.5mL,
答:需要38%的盐酸的体积为32.5mL.
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 8.8g
| 100 |
| x |
| 73 |
| y |
| 44 |
| 8.8g |
x=20g,y=14.6g,
大理石中碳酸钙的质量分数为:
| 20g |
| 24g |
答:大理石中碳酸钙的质量分数为83.3%.
(2)所用稀盐酸溶液的质量为:14.6g÷10%=146g,
答:所用稀盐酸溶液的质量为146g.
(3)设需要38%的盐酸的体积为z,
根据题意有:z×1.1g/cm3×38%=13.6g,
z=32.5mL,
答:需要38%的盐酸的体积为32.5mL.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
下列4个实验方案的设计中,不正确的是( )
| A、用二氧化锰区分水和过氧化氢溶液 |
| B、用水除去CO和CO2混合气体中的CO2 |
| C、用燃着的木条鉴别氧气、空气和二氧化碳3瓶气体 |
| D、在温度不改变的情况下,向一杯硝酸钾溶液中加入硝酸钾可以检验其是否饱和 |
水时生命之源.下面有关水的叙述中,正确的是( )
| A、水汽化时分子间空隙发生了变化 |
| B、用明矾可以鉴别软水和硬水 |
| C、蒸馏、煮沸都能够将自来水变为纯净水 |
| D、保持水的化学性质的最小微粒是氧分子 |
下列所示实验操作正确的是( )
A、 |
B、 |
C、 |
D、 |
水在一定条件下表现出来的下列性质,其中属于化学性质的是( )
| A、能流动 | B、能结冰 |
| C、能分解 | D、能沸腾 |
铁是日常生活中接触最多、用途最广的金属之一.下列有关铁的说法中,错误的是( )
| A、铁在潮湿的空气中会生锈 |
| B、我国政府正在启动的“酱油补铁”工程是为了预防缺铁性贫血 |
| C、生铁放在盐酸中可以完全溶解 |
| D、在铁制品表面镀一层锌可以防止其锈蚀 |
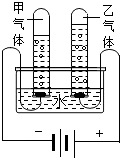 水是生命之源,我们用该了解水、爱护水资源.
水是生命之源,我们用该了解水、爱护水资源.