题目内容
10.如果人体血液中缺乏亚铁离子,就会造成“贫血”,市售出售的某种麦片中含有微量的颗粒很细的还原铁粉,这些铁粉在人体胃液(主要成分稀盐酸)中转化为含有亚铁离子的化合物的化学方程式是Fe+2HCl═FeCl2+H2↑,要起到补铁的效果,该麦片应该密封保存,原因是能和空气中的水和氧气反应生成铁锈.分析 铁能和稀盐酸反应生成氯化亚铁和氢气,能和空气中的水和氧气反应生成铁锈.
解答 解:铁和稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
该麦片应该密封保存,原因是能和空气中的水和氧气反应生成铁锈.
故填:Fe+2HCl═FeCl2+H2↑;能和空气中的水和氧气反应生成铁锈.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列各组物质中,前者是氧化物,后者是混合物的是( )
| A. | 氧化铜、洁净的空气 | B. | 液氧、石灰水 | ||
| C. | 冰水共存物、高锰酸钾 | D. | 氯酸钾、加碘食盐 |
1.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下温度,70℃~80℃时分解生成氧化铜.
Ⅱ.铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应.
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液.
甲同学认为猜想Ⅰ不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
乙同学为验证猜想Ⅱ,进行了如下实验.
【进行实验】
【解释与结论】
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
【反思与评价】
丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下温度,70℃~80℃时分解生成氧化铜.
Ⅱ.铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应.
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液.
甲同学认为猜想Ⅰ不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
乙同学为验证猜想Ⅱ,进行了如下实验.
【进行实验】
| 实验操作 | 实验现象 |
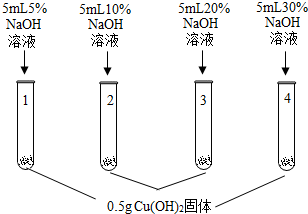 | 1号试管,… 2号试管,蓝色固体不消失 3号试管,蓝色固体减少 4号试管,蓝色固体消失,得到亮蓝色溶液 |
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
【反思与评价】
丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
18.除去下列物质中的少量杂质,方法错误的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | CO | CO2 | 通过足量的氢氧化钠溶液,干燥 |
| B | Cu | Fe | 加入足量的稀硫酸,过滤,洗涤,干燥 |
| C | BaCl2 | Ba(OH)2 | 加入适量的稀硫酸,过滤,洗涤,干燥 |
| D | KCl溶液 | CuCl2 | 加入适量的氢氧化钾溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
5.野外生存训练课上,某同学设计了几种获得饮用水的方法,其中最不合理的是( )
| A. | 融化冰雪,煮沸后使用 | |
| B. | 收集雨水,煮沸后使用 | |
| C. | 用沙子和木炭处理海水,煮沸后使用 | |
| D. | 过滤泥水,煮沸后使用 |
6.“水,不久将成为一个深刻的社会危机”,下列关于水资源的保护,叙述不正确的是( )
| A. | 推动世界各国对水资源进行综合性统筹规划和管理 | |
| B. | 用喷灌、滴灌方法给农作物浇水 | |
| C. | 设法提高工业用水的重复利用率 | |
| D. | 大量开采地下水以满足社会对水的需求 |




 A、B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变,试推断:
A、B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变,试推断: