题目内容
3.水是生命之源,与生活生产关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.(1)下列净水方法中,通常用于除去水中难溶性杂质的是A,净水程度最高的是C.
A.过滤; B.沉淀; C.蒸馏; D.吸附.
(2)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.请写出Ca(HCO3)2受热分解的化学方程式:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑
(3)在水蒸发的过程中,下列说法正确的是A.
A、水分子不断运动; B、水分们之间间隔不变;
C、水分子分解成氢原子和氧原子; D、水分子可以保持水的物理性质.
(4)为了防止水的污染,下列做法有利于保护水资源的是②④.
①抑制水中所有动、植物的生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放.
(5)在化学实验和科学研究中,水也是一种常用的试剂.水分子在特定的条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是AD(填序号).
A、氧元素发生了改变; B、粒子的组成发生了改变;
C、粒子的化学性质发生了改变; D、与水分子相比水合离子的电子数发生了改变.
分析 (1)根据已有的净水的措施解答;
(2)根据化学方程式的书写方法进行分析解答即可;
(3)根据水蒸发的过程中水分子不断运动进行解答;
(4)根据水污染的途径进行解答;
(5)根据水合氢离子的性质进行解答.
解答 解:
(1)过滤能除去水中的不溶性杂质,蒸馏得到的水中不含有任何杂质,是净水程度最高的净水方法,故填:A; C;
(2)碳酸氢钙受热能分解生成碳酸钙沉淀、水和二氧化碳,故填:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
(3)水蒸发的过程中水分子不断运动,故选A;
(4)抑制水中所有动、植物的生长和大量使用化肥农药不利于保护水资源;不任意排放工业废水和生活污水经过净化处理后再排放利于保护水资源;
(5)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+),氧元素没有发生改变,与水分子相比水合离子的电子数相同,没有发生改变,故选:AD.
答案:
(1)A; C;
(2)Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
(3)A;
(4)②④;
(5)AD.
点评 本题考查水的主要性质和用途,要求我们了解水的净化方法和有关爱护水资源的有效做法.

练习册系列答案
相关题目
14.金属M和AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag.则下列说法错误的是( )
| A. | 这个反应属于置换反应 | |
| B. | 金属M可能是铜 | |
| C. | 用M可以回收硝酸银废液中的银 | |
| D. | 反应前后元素M和N化合价发生了变化 |
11.现有液化石油气、天然气、氢气三种物质,根据他们的某种性质可以归为一类.则下列哪种物质可以归入该类( )
| A. | N2 | B. | CO2 | C. | CO | D. | 煤 |
8.以下两幅微观示意图揭示了化学变化的微观实质.相关说法中正确的是( )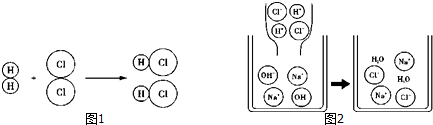

| A. | 图1说明了化学变化前后分子数一定不变 | |
| B. | 原子在化学变化中是可以再分的 | |
| C. | 两幅图表示的都是化合反应 | |
| D. | 图2中H+发生化学变化而Na+没有 |
15.在实验室中,为了探究金属与盐溶液的反应规律,将一定质量的锌粉放入AgNO3与Cu(NO3)2的混合溶液中,实验过程及现象如图所示,结合实际现象判断,以下结论中错误的是( )

| A. | 溶液中一定没有铜离子 | B. | 滤渣中一定含有铜、银 | ||
| C. | 滤渣中可能含有金属锌 | D. | 滤液中主要的溶质含有Zn(NO3)2 |
12.下列物质的性质属于物质的物理性质的是( )
| A. | 浓硝酸的不稳定性 | B. | 氢氧化钾溶液的碱性 | ||
| C. | 硫酸的腐蚀性 | D. | 铁的导电性 |
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: