题目内容
10.区分下列各组物质,所加试剂或操作方法错误的是( )| 选项 | 待区分的物质 | 鉴别方法 |
| A | 合成纤维和纯羊毛 | 取样,分别灼烧,并闻气味 |
| B | CaCl2溶液和NaCl溶液 | 取样,分别加入硝酸银溶液,观察是否产生沉淀 |
| C | 稀盐酸和稀硫酸 | 取样,分别AgNO3溶液,观察是否产生沉淀 |
| D | 碳粉和氧化铜 | 取样,分别加入足量稀硫酸,观察是否能溶解 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据纯羊毛灼烧会产生烧焦羽毛气味的气体进行分析;
B、根据氯离子和银离子会生成氯化银沉淀进行分析;
C、根据氯化银难溶于水,硫酸银微溶于水进行分析;
D、根据金属氧化物会与酸反应生成盐和水进行分析.
解答 解:A、取样品,灼烧,会产生烧焦羽毛气味的是纯羊毛,没有此气味的是合成纤维,现象不同,可以鉴别,故A正确;
B、CaCl2溶液和NaCl溶液,加入硝酸银,都会生成氯化银沉淀,现象相同,不能鉴别,故B错误;
C、氯化银难溶于水,硫酸银微溶于水,取样,分别AgNO3溶液,都会产生沉淀,现象相同,不能鉴别,故C错误;
D、取样,分别加入足量稀硫酸,能溶解的是氧化铜,不能溶解的是碳粉,现象不同,可以鉴别,故D正确.
故选:BC.
点评 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.

练习册系列答案
相关题目
20.老年人骨质疏松,容易骨折,需要多摄入的常量元素是( )
| A. | 钙元素 | B. | 碘元素 | C. | 铁元素 | D. | 锌元素 |
1.下列现象可以用质量守恒定律解释的是( )
| A. | 50g冰融化后,变成水的质量还是50g | |
| B. | 木条燃烧后,灰烬的质量比木条的质量少 | |
| C. | 5g食盐晶体溶于95g水中,溶液的质量为100g | |
| D. | 50mL水和50mL酒精混合后,溶液的体积小于100mL |
5.氯气(Cl2)是黄绿色气体,溶于水时部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO.产物中,次氯酸(HClO)是一种弱酸.氯气溶于水所得溶液称为氯水,它具有很强的漂白性.把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色.晓红同学对“氯水使品红试纸褪色”产生浓厚兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】猜想1:氯水中的水使品红试纸褪色; 猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色; 猜想4:氯水中的HClO使品红试纸褪色.
【实验探究】
【结论】学习小组通过讨论,找到了氯水中使品红试纸褪色的物质.
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是先变红后褪色.
【拓展】铁能在氯气中燃烧生成氯化铁,请写出该反应的化学方程式2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】猜想1:氯水中的水使品红试纸褪色; 猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色; 猜想4:氯水中的HClO使品红试纸褪色.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| ①把品红试纸放入水中 | 试纸不褪色 | 猜想1不成立 |
| ②把品红试纸放在干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
| ③把品红试纸放入盐酸中 | 试纸不褪色 | 猜想3不成立 |
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是先变红后褪色.
【拓展】铁能在氯气中燃烧生成氯化铁,请写出该反应的化学方程式2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
15.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如图: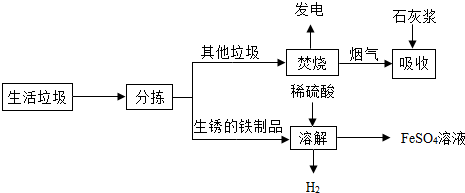
资料1:垃圾焚烧产生烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:
(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是2HCl+Ca(OH)2═CaCl2+2H2O;(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示:(仅在56.7℃或64℃温度下可同时析出两种晶体).
若需从硫酸亚铁溶液中结晶出FeSO4•4H2O,应控制的结晶温度(t)的范围为不超过64℃;
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑;
(7)请你就扬州市生活垃圾处理提一条建议生活垃圾分类回收等.

资料1:垃圾焚烧产生烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:
(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是2HCl+Ca(OH)2═CaCl2+2H2O;(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示:(仅在56.7℃或64℃温度下可同时析出两种晶体).
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑;
(7)请你就扬州市生活垃圾处理提一条建议生活垃圾分类回收等.
20.填写下列表格(“混合物”栏中括号内为杂质):
| 混合物 | 除去杂质的化学方程式 |
| 铜粉(Fe) | Fe+2HCl=FeCl2+H2↑(合理即可) |
| FeCl2溶液(CuCl2) | Fe+CuCl2=Cu+FeCl2 |
