题目内容
13.如图是一氧化碳还原氧化铜的实验装置.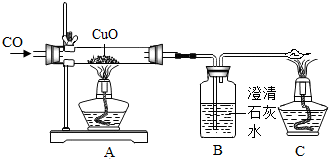
(1)装置A中的现象是黑色粉末逐渐变成红色,反应方程式是CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(2)装置B中的现象是澄清石灰水变浑浊,反应方程式是Ca(OH)2+CO2=CaCO3↓+H2O.
(3)装置C的作用是除去未反应完的一氧化碳,避免污染空气.
分析 根据一氧化碳还原氧化铜的产物分析反应的现像,写化学方程式;根据一氧化碳的毒性及可燃性分析.
解答 解:(1)一氧化碳具有还原性,能和氧化铜反应生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以A处观察到的现象是:黑色固体变成红色,化学方程式为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(2)一氧化碳与氧化铜反应,黑色粉末变成红色,生成的二氧化碳使澄清石灰水变浑浊;装置B中的现象是澄清石灰水变浑浊,化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
(3)一氧化碳有毒,不能直接排放到空气中,因此C处放置点燃的酒精灯的目的是燃烧尾气中的CO,防止污染空气.
故答案为:
(1)黑色粉末逐渐变成红色;CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
(2)澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O
(3)除去未反应完的一氧化碳,避免污染空气
点评 在使用可燃性气体进行实验前,一定要检验气体纯度,防止气体不纯而引起爆炸.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
3.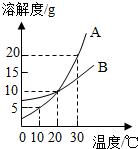 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )| A. | 30℃时,将B物质的不饱和溶液转变为饱和溶液,可以采取恒温蒸发溶剂的方法 | |
| B. | A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 | |
| C. | B物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小 | |
| D. | 30℃时,向100克水中加入25克A物质,充分溶解后所得溶液是饱和溶液 |
1.下列电离方程式中,正确的是( )
| A. | Ca(OH)2═Ca2++(OH)2- | B. | H2SO4═H2++SO42- | ||
| C. | Al2(SO4)3═2Al3++3SO42- | D. | NaCl═Na+1+Cl-1 |
18.下列描述属于氧气化学性质的是( )
| A. | 通常状况下,氧气是无色、无味的气体 | |
| B. | 通过低温加压,可使氧气液化成淡蓝色的液体 | |
| C. | 氧气的密度比空气大,可用向上排空气法收集 | |
| D. | 氧气是一种性质比较活泼的气体,能氧化许多物质 |
7.下列物质按混合物、化合物.氧化物、单质的顺序排列的是( )
| A. | 石油 铝合金 干冰 石墨 | B. | 汽水 煤 二氧化碳 金刚石 | ||
| C. | 空气 碳酸钙 蒸馏水 液氧 | D. | 天然气 石灰石 氧化铜 锌 |